Les packages SEND entièrement assemblés sont libérés de la cellule pour être collectés pour la thérapie génique. Crédit : Institut McGovern
Composé de composants trouvés dans le corps humain, le système programmable est une étape vers une administration plus sûre et ciblée de l’édition de gènes et d’autres thérapies moléculaires.
Des chercheurs de AVEC, le McGovern Institute for Brain Research du MIT, le Howard Hughes Medical Institute et le Broad Institute du MIT et de Harvard ont développé une nouvelle façon d’administrer des thérapies moléculaires aux cellules. Le système, appelé SEND, peut être programmé pour encapsuler et fournir différents ARN cargaisons. SEND exploite des protéines naturelles dans le corps qui forment des particules de type virus et se lient à l’ARN, et il peut provoquer une réponse immunitaire moindre que d’autres approches d’administration.
La nouvelle plate-forme d’administration fonctionne efficacement dans les modèles cellulaires et, avec un développement ultérieur, pourrait ouvrir une nouvelle classe de méthodes d’administration pour un large éventail de médicaments moléculaires, notamment ceux destinés à l’édition et au remplacement de gènes. Les véhicules d’administration existants pour ces thérapies peuvent être inefficaces et s’intégrer de manière aléatoire dans le génome des cellules, et certains peuvent stimuler des réactions immunitaires indésirables. SEND a la promesse de surmonter ces limitations, ce qui pourrait ouvrir de nouvelles opportunités pour déployer la médecine moléculaire.
https://www.youtube.com/watch?v=FPHANhbqJZg
Des chercheurs du MIT, du McGovern Institute for Brain Research du MIT, du Howard Hughes Medical Institute et du Broad Institute du MIT et de Harvard ont développé une nouvelle façon de fournir des thérapies moléculaires aux cellules. Crédit : Produit par le McGovern Institute et Opus Design en collaboration avec Feng Zhang, Rhiannon Macrae et le Broad Institute.
« La communauté biomédicale a développé de puissantes thérapies moléculaires, mais les délivrer aux cellules de manière précise et efficace est un défi », a déclaré Feng Zhang, pionnier du CRISPR, auteur principal de l’étude, membre de l’institut principal du Broad Institute, chercheur au McGovern. Institute, et le professeur James et Patricia Poitras de neurosciences au MIT. « SEND a le potentiel pour surmonter ces défis. » Zhang est également chercheur au Howard Hughes Medical Institute et professeur aux départements des sciences du cerveau et cognitives et du génie biologique du MIT.
Rapports dans Science, l’équipe décrit comment SEND (Sélectif Ee endogèneNcapsidation pour cellulaire réelivery) tire parti des molécules fabriquées par les cellules humaines. Au centre de SEND se trouve une protéine appelée PEG10, qui se lie normalement à son propre ARNm et forme une capsule protectrice sphérique autour d’elle. Dans leur étude, l’équipe a conçu le PEG10 pour conditionner et délivrer sélectivement d’autres ARN. Les scientifiques ont utilisé SEND pour fournir le système d’édition de gènes CRISPR-Cas9 à des cellules de souris et humaines afin d’éditer des gènes ciblés.
Le premier auteur, Michael Segel, chercheur postdoctoral dans le laboratoire de Zhang, et Blake Lash, deuxième auteur et étudiant diplômé du laboratoire, ont déclaré que le PEG10 n’est pas unique dans sa capacité à transférer l’ARN. “C’est ce qui est si excitant”, a déclaré Segel. « Cette étude montre qu’il existe probablement d’autres systèmes de transfert d’ARN dans le corps humain qui peuvent également être exploités à des fins thérapeutiques. Cela soulève également des questions vraiment fascinantes sur les rôles naturels de ces protéines. »
Inspiration de l’intérieur
La protéine PEG10 existe naturellement chez l’homme et est dérivée d’un « rétrotransposon » – un élément génétique semblable à un virus – qui s’est intégré dans le génome des ancêtres humains il y a des millions d’années. Au fil du temps, le PEG10 a été coopté par l’organisme pour faire partie du répertoire des protéines importantes pour la vie.
Il y a quatre ans, les chercheurs ont montré qu’une autre protéine dérivée des rétrotransposons, l’ARC, forme des structures ressemblant à des virus et est impliquée dans le transfert d’ARN entre les cellules. Bien que ces études aient suggéré qu’il pourrait être possible de concevoir des protéines de rétrotransposon comme plate-forme de livraison, les scientifiques n’avaient pas réussi à exploiter ces protéines pour emballer et livrer des cargaisons d’ARN spécifiques dans des cellules de mammifères.
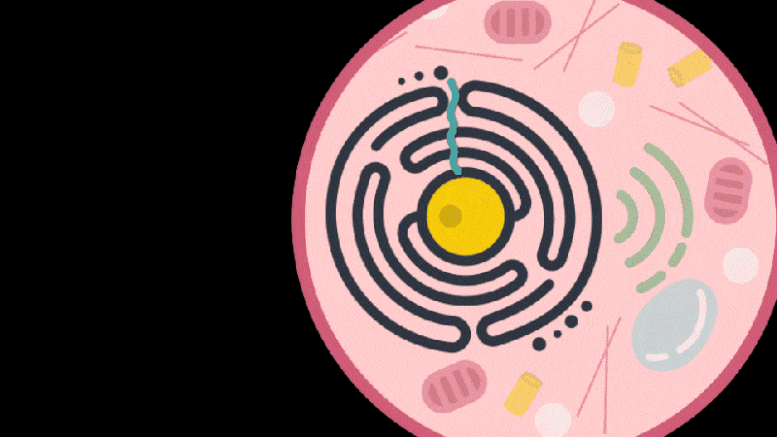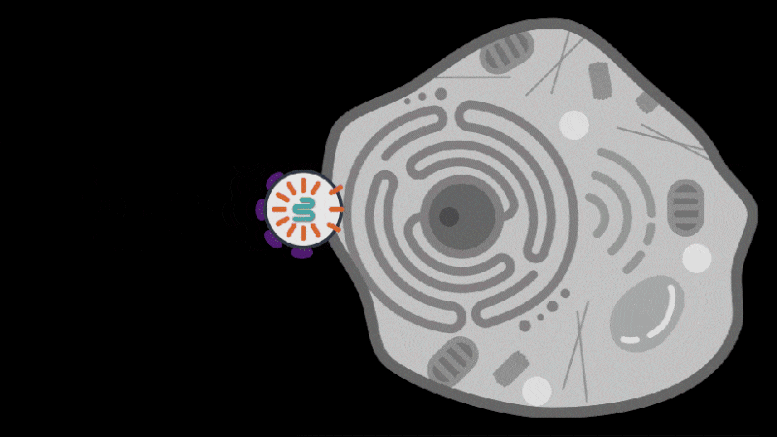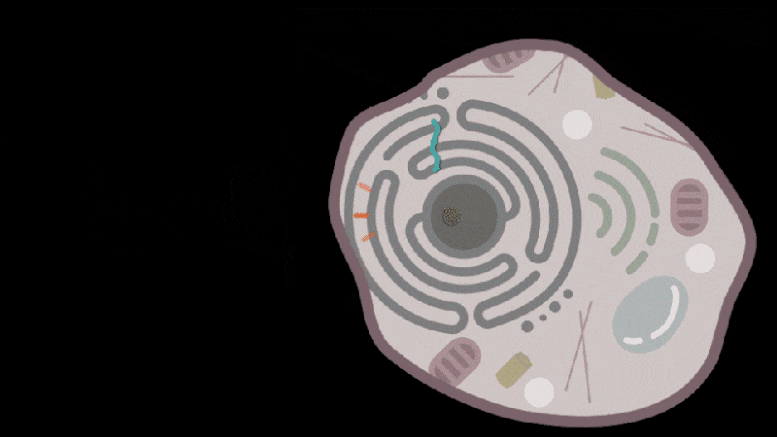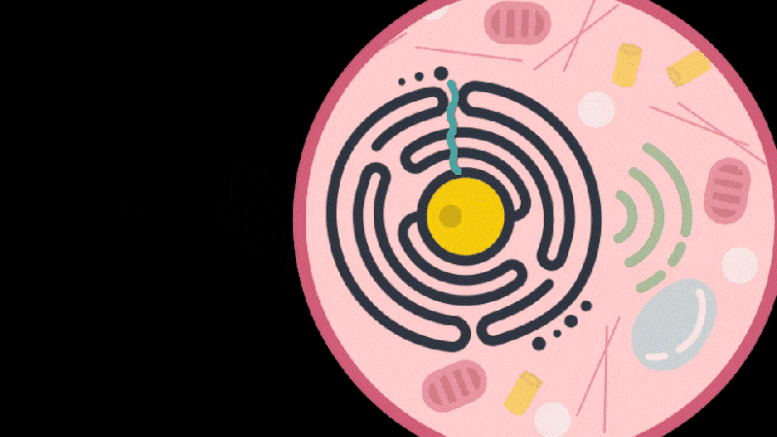
Les packages SEND sont introduits dans les cellules malades pour délivrer un ARNm thérapeutique et restaurer la santé. Crédit : Institut McGovern
Sachant que certaines protéines dérivées de rétrotransposons sont capables de se lier et de conditionner une cargaison moléculaire, l’équipe de Zhang s’est tournée vers ces protéines comme véhicules de livraison possibles. Ils ont systématiquement recherché dans ces protéines du génome humain celles qui pourraient former des capsules protectrices. Dans leur analyse initiale, l’équipe a trouvé 48 gènes humains codant pour des protéines qui pourraient avoir cette capacité. Parmi celles-ci, 19 protéines candidates étaient présentes chez les souris et les humains. Dans la lignée cellulaire étudiée par l’équipe, le PEG10 s’est imposé comme une navette efficace ; les cellules ont libéré significativement plus de particules de PEG10 que toute autre protéine testée. Les particules de PEG10 contenaient également principalement leur propre ARNm, ce qui suggère que le PEG10 pourrait être capable d’empaqueter des molécules d’ARN spécifiques.
Développement d’un système modulaire
Pour développer la technologie SEND, l’équipe a identifié les séquences moléculaires, ou « signaux », dans l’ARNm de PEG10 que PEG10 reconnaît et utilise pour emballer son ARNm. Les chercheurs ont ensuite utilisé ces signaux pour concevoir à la fois le PEG10 et d’autres cargaisons d’ARN afin que le PEG10 puisse emballer sélectivement ces ARN. Ensuite, l’équipe a décoré les capsules de PEG10 avec des protéines supplémentaires, appelées « fusogènes », qui se trouvent à la surface des cellules et les aident à fusionner.
En créant les fusogènes sur les capsules de PEG10, les chercheurs devraient pouvoir cibler la capsule sur un type particulier de cellule, de tissu ou d’organe. Dans un premier temps vers cet objectif, l’équipe a utilisé deux fusogènes différents, dont un trouvé dans le corps humain, pour permettre la livraison de la cargaison SEND.
« En mélangeant et en faisant correspondre différents composants du système SEND, nous pensons qu’il fournira une plate-forme modulaire pour développer des thérapies pour différentes maladies », a déclaré Zhang.
Faire progresser la thérapie génique
SEND est composé de protéines produites naturellement dans le corps, ce qui signifie qu’il peut ne pas déclencher de réponse immunitaire. Si cela est démontré dans d’autres études, les chercheurs affirment que SEND pourrait ouvrir des opportunités pour fournir des thérapies géniques à plusieurs reprises avec des effets secondaires minimes. « La technologie SEND complétera les vecteurs de livraison virale et les nanoparticules lipidiques pour élargir davantage la boîte à outils des moyens de fournir des thérapies géniques et d’édition aux cellules », a déclaré Lash.
Ensuite, l’équipe testera SEND sur des animaux et perfectionnera le système pour livrer une cargaison à une variété de tissus et de cellules. Ils continueront également à sonder la diversité naturelle de ces systèmes dans le corps humain afin d’identifier d’autres composants pouvant être ajoutés à la plate-forme SEND.
« Nous sommes ravis de continuer à faire avancer cette approche », a déclaré Zhang. « La réalisation que nous pouvons utiliser le PEG10, et très probablement d’autres protéines, pour concevoir une voie d’administration dans le corps humain afin de conditionner et d’administrer de nouveaux ARN et d’autres thérapies potentielles est un concept vraiment puissant. »
Référence : « La protéine de type rétrovirus de mammifère PEG10 emballe son propre ARNm et peut être pseudotypée pour la livraison de l’ARNm » par Michael Segel, Blake Lash, Jingwei Song, Alim Ladha, Catherine C. Liu, Xin Jin, Sergei L. Mekhedov, Rhiannon K. Macrae, Eugene V. Koonin et Feng Zhang, 20 août 2021, Science.
DOI : 10.1126/science.abg6155
Ce travail a été rendu possible grâce au soutien du Simons Center for the Social Brain du MIT ; Programme de recherche intra-muros des National Institutes of Health; Les National Institutes of Health accordent 1R01-HG009761 et 1DP1-HL141201 ; Institut médical Howard Hughes; Philanthropie ouverte ; Fondation caritative G. Harold et Leila Y. Mathers; Fondation Edward Mallinckrodt, Jr. ; Centre de recherche sur les troubles psychiatriques de Poitras au MIT ; Centre de recherche sur l’autisme Hock E. Tan et K. Lisa Yang au MIT ; Yang-Tan Center for Molecular Therapeutics au MIT; Lisa Yang ; famille Phillips; R. Metcalfe; et J. et P. Poitras.