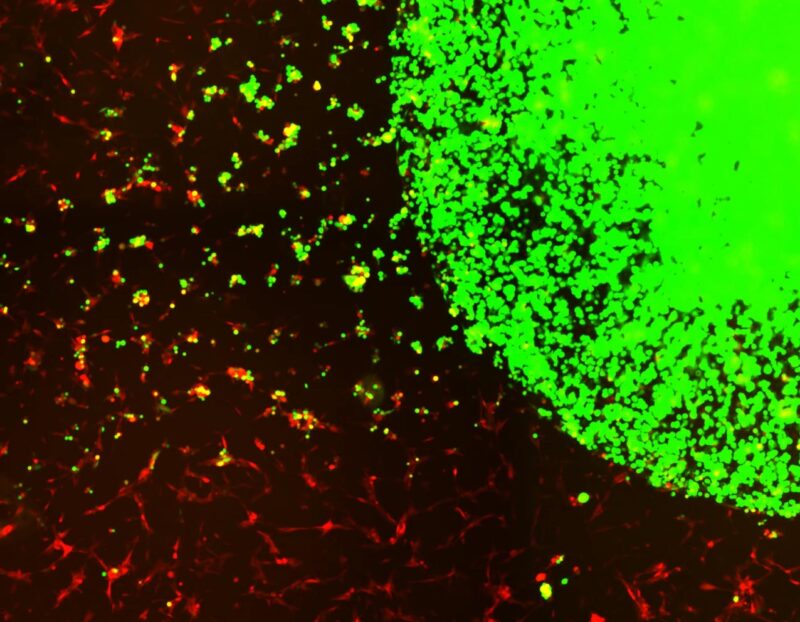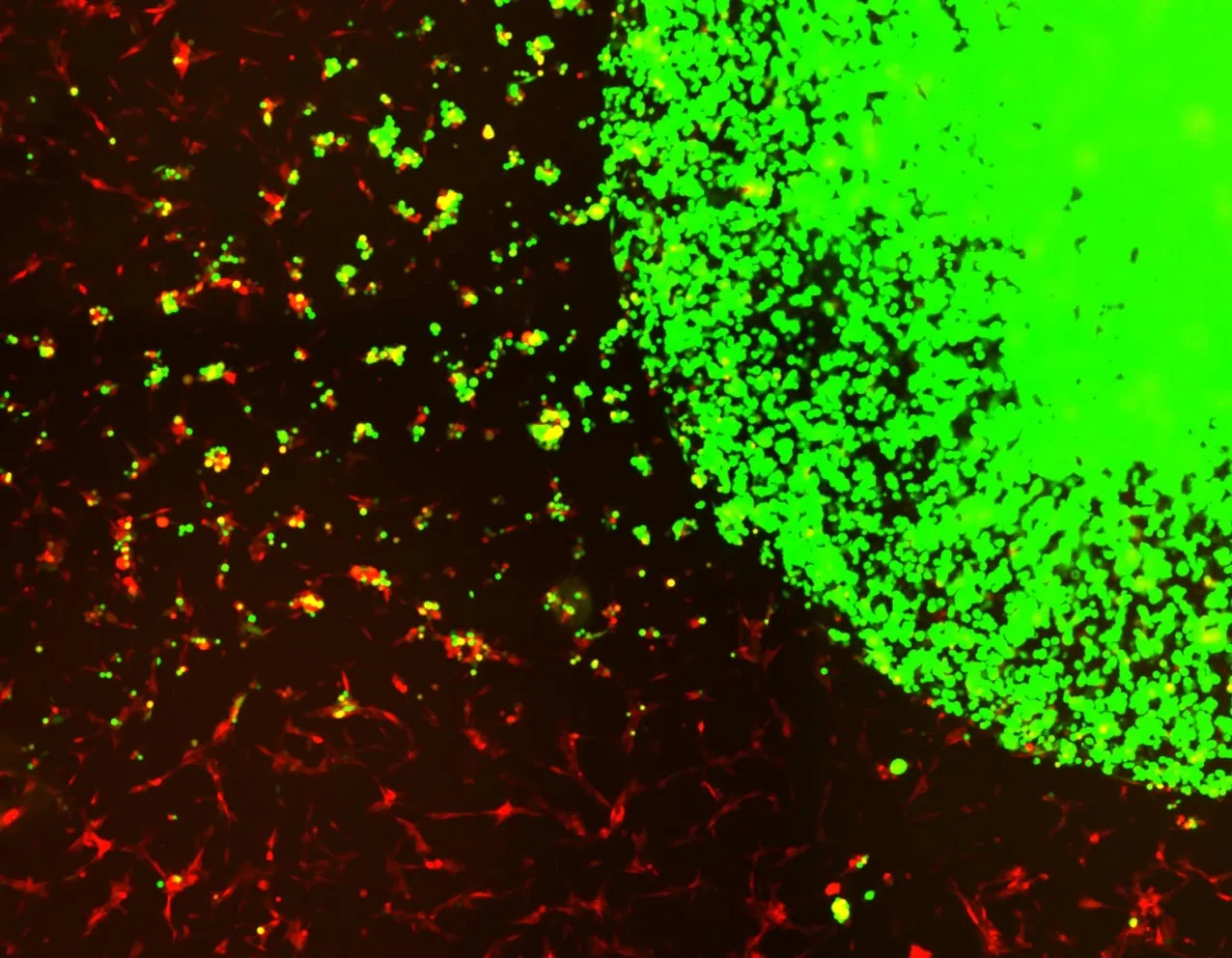
Cellules souches encapsulées (vert) traquant et tuant les cellules tumorales du GBM (rouge). Crédit : laboratoire Shah (CSTI)
Les chercheurs ont découvert une méthode de diagnostic pour identifier les récepteurs des cellules cancéreuses dans le sang, puis ont conçu une thérapie cellulaire pour cibler et tuer les cellules tumorales dans le cerveau, ouvrant ainsi la voie aux essais cliniques.
Les glioblastomes (GBM) sont des tumeurs cancéreuses très agressives du cerveau et de la moelle épinière. Les cancers du cerveau tels que les GBM sont difficiles à traiter car de nombreux médicaments anticancéreux ne peuvent pas traverser la barrière hémato-encéphalique et plus de 90 % des tumeurs GBM réapparaissent après une ablation chirurgicale, bien que la chirurgie et les chimiothérapies et radiothérapies ultérieures constituent le meilleur moyen de traiter la maladie. Dans une nouvelle étude dirigée par des chercheurs du Brigham and Women’s Hospital et de la Harvard Medical School, des scientifiques ont mis au point une nouvelle stratégie thérapeutique pour traiter les GBM après une intervention chirurgicale en utilisant des cellules souches prélevées sur des donneurs sains et modifiées pour attaquer les cellules tumorales spécifiques des GBM. Cette stratégie a démontré une grande efficacité dans des modèles précliniques de GBM, 100 % des souris vivant plus de 90 jours après le traitement. Les résultats seront publiés aujourd’hui (19 mai 2022) dans le journal Nature Communications.
Il s’agit de la première étude à notre connaissance qui identifie les récepteurs cibles sur les cellules tumorales avant d’initier la thérapie, et qui utilise une thérapie biodégradable, encapsulée dans un gel, basée sur des cellules souches artificielles “prêtes à l’emploi” après une chirurgie de la tumeur GBM”, a déclaré Khalid Shah, MS, PhD, directeur du Center for Stem Cell and Translational Immunotherapy (CSTI) et vice-président de la recherche au département de neurochirurgie de la Brigham Medical School et du Harvard Stem Cell Institute (HSCI).
“À l’avenir, nous appliquerons cette stratégie pour identifier rapidement les récepteurs cibles après avoir reçu un diagnostic de GBM, puis nous administrerons une thérapie à base de cellules souches artificielles encapsulées dans un gel, disponible dans le commerce, à partir d’un réservoir préfabriqué.”
De nombreuses thérapies cellulaires contre le cancer sont dérivées des cellules souches ou des cellules immunitaires du patient. Cependant, dans le cas d’une maladie comme le GBM, la plupart des patients sont opérés dans la première semaine suivant le diagnostic en raison de la progression rapide de la maladie, ce qui laisse peu de temps pour développer des thérapies à partir de leurs propres types de cellules. Au lieu de cela, les scientifiques ont mis au point une nouvelle approche consistant à utiliser des cellules souches allogènes, c’est-à-dire des cellules provenant d’individus sains, de sorte que le remède soit disponible et puisse être administré immédiatement au moment de l’opération. Shah et ses collègues ont évalué l’efficacité de plusieurs capsules qui transportent le traitement à base de cellules souches dans le cerveau et ont trouvé une capsule d’hydrogel biodégradable qui transporte avec succès le traitement sans être emporté par le liquide céphalo-rachidien.
Les chercheurs ont d’abord identifié des récepteurs spéciaux appelés “récepteurs de mort” sur les cellules tumorales circulantes (CTC) – ou cellules cancéreuses dans le sang – en utilisant un biomarqueur génétique couramment exprimé sur les cellules tumorales. Une fois ces récepteurs identifiés, ils ont prélevé des cellules souches dans la moelle osseuse de donneurs humains sains et les ont modifiées pour qu’elles libèrent une protéine qui se lie aux récepteurs de mort et déclenche la mort cellulaire. Ils ont également intégré au système de cellules souches un interrupteur de sécurité qui permet de suivre les cellules souches par imagerie TEP et qui, lorsqu’il est activé, éradique les cellules souches et renforce encore la mort des cellules cancéreuses. Enfin, l’équipe de Shah a évalué l’efficacité des cellules thérapeutiques bifonctionnelles (MSCBif) dans des modèles animaux de tumeurs primaires et récurrentes de GBM après chirurgie.
Notamment, toutes les souris qui ont reçu le gel thérapeutique à base de cellules souches encapsulées après la chirurgie étaient encore en vie 90 jours après le traitement, par rapport aux souris qui ont uniquement subi une chirurgie, qui ont présenté une durée de survie moyenne de 55 jours. Les chercheurs ont en outre évalué la sécurité de ce traitement clinique en menant plusieurs études utilisant différentes doses de la thérapie MSC sur des souris. Ils n’ont trouvé aucun signe de toxicité chez les souris avec ou sans tumeurs.
Les résultats de l’étude ouvrent la voie à des essais cliniques de phase I chez des patients atteints de GBM devant subir une opération du cerveau dans les deux prochaines années. Shah et ses collègues notent que cette stratégie thérapeutique sera applicable à un plus grand nombre de tumeurs solides et que des recherches supplémentaires sur ses applications sont justifiées.
“Au-delà du taux de réussite significatif de cette thérapie, ces résultats suggèrent que nous pouvons utiliser des cellules souches provenant d’individus sains pour traiter des patients atteints de cancer”, a déclaré Shah. “Ce travail jette les bases pour commencer à construire une biobanque de cellules souches thérapeutiques ciblant différents récepteurs sur les cellules tumorales et le système immunitaire.cellules dans le microenvironnement tumoral que nous pourrons un jour utiliser pour traiter un large éventail de cancers difficiles à traiter comme le GBM”.
Référence : “Identification des récepteurs cibles et traitement ultérieur des tumeurs cérébrales réséquées avec des cellules souches allogéniques encapsulées et modifiées” 19 mai 2022, Nature Communications.
DOI: 10.1038/s41467-022-30558-3
Financement : Cette étude a été soutenue par le Fonds de Recherche et AMASA Therapeutics.
Divulgations : Shah détient une participation dans AMASA Therapeutics et est membre du conseil d’administration de cette société qui développe des thérapies à base de cellules souches pour le cancer. Le co-auteur Deepak Bhere détient une participation dans AMASA Therapeutics et est consultant auprès de cette société.