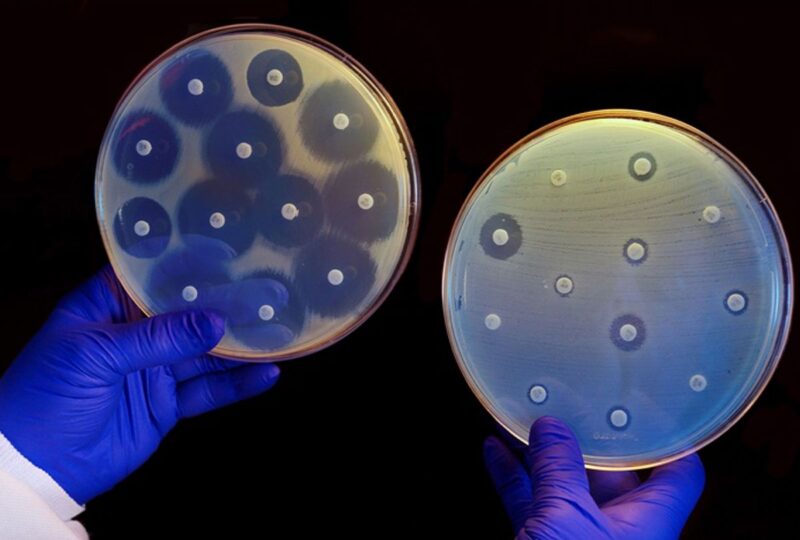
Oubliez pour l’instant le COVID-19, la variole du singe et d’autres virus et considérez une autre menace qui inquiète les spécialistes des maladies infectieuses : les infections urinaires courantes, ou UTI, qui entraînent des visites aux urgences et même des hospitalisations en raison de l’échec des antibiotiques oraux.
Il n’y a pas d’Opération Warp Speed pour nous sauver des germes qui causent ces infections, qui ont étendu leur champ d’action au cours de la première année de la pandémie, selon un nouveau rapport des Centers for Disease Control and Prevention. L’année dernière, la FDA a refusé d’approuver deux médicaments oraux prometteurs – le sulopenem et le tebipenem – pour traiter les infections urinaires résistantes aux médicaments, affirmant qu’elle avait besoin de davantage de preuves qu’ils fonctionnaient aussi bien que les médicaments actuels.
En attendant, certains patients atteints d’infections urinaires “doivent être admis et recevoir un traitement par voie intraveineuse pour une infection de la vessie qui serait normalement traitée par des antibiotiques oraux”, a déclaré le Dr Sarah Doernberg, spécialiste des maladies infectieuses au centre médical de l’université de Californie-San Francisco.
Rebecca Clausen, employée de bureau à Durham, en Caroline du Nord, s’est vu prescrire plusieurs traitements d’un antibiotique oral bon marché pour une infection urinaire persistante au début de l’année, mais elle semblait “revenir sans cesse”, dit-elle. Les médecins ont envisagé un traitement de six semaines avec un médicament intraveineux, l’ertapenem, qui lui aurait coûté environ 2 000 dollars, mais ils ont décidé que cela ne servirait probablement à rien. Pour l’instant, elle espère simplement que l’infection ne s’aggravera pas.
Bien que les spécialistes affirment qu’ils voient de plus en plus d’infections urinaires que les antibiotiques oraux ne peuvent pas éliminer, le problème est encore considéré comme relativement rare (les responsables fédéraux de la santé ne suivent pas directement cette question). Cependant, il est emblématique d’une défaillance de l’industrie des antibiotiques qui, selon les experts et même les sénateurs américains, ne peut être résolue que par l’intervention du gouvernement.
Le rapport du CDC, publié le 12 juillet, montre qu’après avoir diminué au cours de la décennie précédente, les taux d’incidence de sept organismes résistants aux antimicrobiens mortels ont augmenté de 15 % en moyenne dans les hôpitaux en 2020, en raison de la surutilisation de ces organismes chez les patients sous COVID. Certaines des croissances les plus fortes ont été observées chez des organismes qui provoquent des infections urinaires difficiles à traiter.
Bien que près de 50 000 Américains – et environ 1,3 million de personnes dans le monde – meurent chaque année d’infections bactériennes résistantes, la FDA n’a pas approuvé de nouvel antibiotique depuis 2019. Big Pharma a pour la plupart abandonné le développement des antibiotiques, et sept des 12 entreprises qui ont réussi à mettre un médicament sur le marché au cours de la dernière décennie ont fait faillite ou ont quitté le secteur des antibiotiques en raison de mauvaises ventes.
Cela s’explique par un paradoxe central : plus un antibiotique est administré, plus les bactéries mutent rapidement pour le contourner. Les praticiens réduisent donc agressivement l’utilisation des médicaments, 90 % des hôpitaux américains mettant en place des programmes d’intendance pour limiter l’utilisation des antibiotiques, y compris les nouveaux. Cela a entraîné une perte d’intérêt des investisseurs pour l’industrie des antibiotiques.
Un pipeline de nouveaux médicaments est vital, étant donné la capacité implacable des bactéries à muter et à s’adapter. Mais si la résistance est un danger permanent, quelque 90 à 95 % des infections mortelles impliquent des microbes qui ne sont pas multirésistants mais difficiles à traiter pour d’autres raisons, comme l’état délicat du patient, a déclaré le Dr Sameer Kadri, chef de l’épidémiologie clinique au département de médecine des soins intensifs du centre clinique des National Institutes of Health.
“Aussi mauvaise que soit la résistance aux antibiotiques, elle est mauvaise contre une minorité de personnes”, a déclaré Jason Gallagher, professeur et pharmacien spécialisé dans les maladies infectieuses à l’hôpital universitaire Temple de Philadelphie. Comme les cliniciens ne peuvent généralement pas déterminer rapidement le niveau de résistance d’un microbe, ils commencent la plupart du temps avec l’ancien médicament. “Cela fait des anti-infectieux un investissement assez difficile du point de vue des entreprises pharmaceutiques”, a-t-il ajouté. “Vous allez développer votre médicament et les gens vont faire de leur mieux pour ne pas l’utiliser”.
Selon le Dr David Shlaes, scientifique retraité de l’industrie pharmaceutique, la disparition des sociétés d’antibiotiques entraîne celle de leur expertise scientifique. Si un modèle de résistance particulièrement mortel devait se développer en l’absence d’un pipeline de médicaments, il pourrait causer une destruction à une échelle effrayante, a-t-il dit.
“Les antibiotiques sont un élément essentiel de la civilisation”, a déclaré Kevin Outterson, un professeur de droit de l’Université de Boston qui dirige un fonds public-privé qui aide les entreprises à développer des antimicrobiens. “Ils doivent être renouvelés à chaque génération ou nous glisserons à nouveau dans l’ère pré-antibiotique”.
Les obstacles à l’approbation des médicaments contre l’infection urinaire, le tébipénème et le sulopénème, illustrent la complexité et les défis réglementaires de l’arène des antibiotiques.
Dans un grand essai clinique achevé l’année dernière, IterumLe sulopénème de Therapeutics s’est avéré bien meilleur qu’un médicament plus ancien, la ciprofloxacine, pour réduire les symptômes de l’infection urinaire, mais il n’a pas semblé aussi efficace pour tuer les bactéries, ce que la FDA considère comme un critère de réussite tout aussi important. Lors d’un atelier organisé le 3 juin, les responsables de la FDA ont indiqué qu’ils pourraient être disposés à modifier leur norme lors de futurs essais.
Une autre société, Spero Therapeutics, a publié ce qui semblait être un essai réussi pour le tébipénème oral dans le New England Journal of Medicine en avril. Mais les responsables de la FDA ont rejeté la demande de licence de Spero parce qu’une espèce de bactérie incluse dans l’analyse a été jugée non pertinente pour l’efficacité du médicament.
Une bouée de sauvetage pour les patients
Bien que de nouveaux médicaments oraux contre les infections urinaires fassent cruellement défaut, les médicaments IV peuvent encore venir à bout de la plupart des infections urinaires de routine. Mais la menace plus large d’un avenir sans nouveaux antibiotiques est particulièrement effrayante pour les patients atteints de maladies chroniques graves, qui sont en permanence engagés dans une lutte contre les bactéries.
Deux ou trois fois par jour, Molly Pam, une cuisinière de 33 ans qui défend les intérêts des patients à San Francisco, inhale des doses de colistine ou d’aztréonam par nébulisation. Ce sont des antibiotiques que le commun des mortels évite, mais pour les 30 000 patients américains atteints de mucoviscidose comme Pam, les microbes mortels et les médicaments puissants font partie du quotidien.
Plusieurs fois par an, lorsque la fièvre ou l’épuisement signalent que les microbes qui colonisent ses poumons endommagés et obstrués par le mucus deviennent excessivement procréateurs, Pam se rend dans une clinique ou un hôpital pour un traitement par intraveineuse. En 2019, alors qu’elle s’approche de la résistance à tous les antibiotiques, le médicament Zerbaxa reçoit l’approbation de la FDA.
Les bactéries Pseudomonas et MRSA ont colonisé les poumons de Pam depuis son enfance, leurs mutations nécessitant des mises à jour fréquentes des antibiotiques. En 2018, elle a été frappée par une bactérie résistante aux médicaments, semblable à la tuberculose, qui a nécessité un an de traitements médicamenteux IV trois fois par jour en plus de ses autres médicaments. L’année dernière, elle a été transportée par avion au Stanford Medical Center après avoir commencé à cracher du sang provenant d’un poumon endommagé.
Les médecins analysent les crachats de Pam quatre fois par an pour déterminer quels sont les microbes qu’elle héberge et quels antibiotiques seront efficaces contre eux. Elle n’est toujours qu’à quelques mutations du désastre.
“Je suis absolument dépendante des nouveaux médicaments”, a déclaré Pam.
Programmes de pilotage de l’intendance
Le développement et l’essai de ces nouvelles molécules est un terrain difficile, avec des conflits fréquents entre la FDA et l’industrie sur la façon de mesurer l’efficacité d’un antibiotique – est-ce la survie du patient ? L’amélioration des symptômes ? Le nombre de bactéries ? Et sur quelle période ?
Entre-temps, le Congrès a aidé l’industrie en prolongeant les brevets, et les agences fédérales ont versé des centaines de millions de dollars en subventions et en partenariats. L’Organisation mondiale de la santé et l’industrie pharmaceutique ont créé en 2020 un fonds de capital-risque d’un milliard de dollars pour soutenir les entreprises d’antibiotiques méritantes.
Pourtant, l’intendance des antibiotiques a sans doute eu la plus grande influence sur la réduction de la menace de la résistance. Un rapport des CDC de 2019 a révélé une réduction de 18 % depuis 2013 des décès causés par des organismes résistants aux médicaments, et une baisse de 21 % des infections de SARM, ou résistants à la méthicilline. Staphylococcus aureusqui était autrefois le croque-mitaine de la médecine.
Mais le progrès peut rendre plus difficile l’essai de nouveaux médicaments. Les infections bactériennes hautement résistantes étant encore relativement rares, les essais cliniques des nouveaux médicaments mesurent généralement leur efficacité contre toutes les bactéries de la classe concernée, plutôt que contre les microbes les plus résistants.
Et comme les nouveaux médicaments sont souvent approuvés simplement en montrant qu’ils sont à peu près aussi efficaces que les médicaments existants, les médecins spécialisés dans les maladies infectieuses les évitent généralement, du moins au début, sceptiques quant à leur prix relativement élevé et leur supériorité douteuse.
“Il n’y a pas tant de personnes que cela qui présentent une résistance aux antibiotiques”, a déclaré le Dr Emily Spivak, qui dirige les programmes de gestion des maladies à l’Université de l’Utah et aux hôpitaux VA de Salt Lake City. “Lorsque les gens contractent ces infections, c’est horrible. Mais il n’y en a pas assez pour faire le genre de profits que les entreprises veulent.”
Par exemple, les patients hospitalisés atteints de pneumonie liée au SARM peuvent souvent être traités avec de la vancomycine (à partir d’environ 15 dollars par jour), a déclaré Mme Spivak, qui préside le comité sur la résistance aux antimicrobiens de l’Infectious Diseases Society of America. Elle se tourne parfois vers une alternative plus récente, la ceftaroline (400 dollars par jour), qui peut avoir moins d’effets secondaires. “Mais même ainsi, nous ne faisons pas le plein de ces médicaments, et nous ne le ferons jamais, car heureusement nous pouvons faire d’autres choses pour prévenir le SARM, comme nettoyer la peau avant une opération et garder les cathéters propres.”
L’heure de la “vitesse de distorsion” ?
Dans les premiers jours du COVID, de nombreux hôpitaux ont désespérément jeté des antimicrobiens sur le mystérieux virus, et lesLa crise pandémique a mis à rude épreuve les équipes d’intendance, a déclaré M. Spivak. Les nouvelles données du CDC montrent que les cliniciens ont donné des antibiotiques à 80 % des patients hospitalisés pour le COVID au cours des huit premiers mois de la pandémie, bien que ces médicaments n’aient aucun impact sur l’infection par le COVID.
Mais l’adoption de nouveaux antibiotiques a été lente. Un rapport sur 17 nouveaux antibiotiques commercialisés aux Etats-Unis au cours des cinq dernières années a montré que seuls trois d’entre eux avaient des ventes supérieures à 100 millions de dollars par an. Les 17 ont enregistré des ventes moyennes d’environ 44 millions de dollars pour les 12 mois se terminant en juin 2020.
Quelques-uns des nouveaux médicaments, comme un antibiotique combiné commercialisé aux États-Unis sous le nom d’Avycaz, ont progressivement remplacé la colistine, un composé hautement toxique des années 1950 qui a été réintroduit en 2000 en raison de son efficacité contre certaines bactéries résistantes.
Pourtant, même cette transition, recommandée par les spécialistes des maladies infectieuses, a été progressive. Ce n’est pas surprenant puisque la colistine coûte environ 140 $ pour un traitement de 10 jours, alors qu’un traitement à l’Avycaz peut coûter de 14 000 $ à 28 000 $ à un hôpital, a fait remarquer Dominic Chan, chef des services pharmaceutiques à Legacy Health, dans l’Oregon.
Le remboursement de Medicare pour le traitement des infections hospitalières est faible, a déclaré M. Chan, “il n’y a donc aucune incitation pour les hôpitaux à investir ce type de capital dans l’introduction de ces agents, si ce n’est pour faire ce qu’il faut.”
Dans la plupart des cas, les hôpitaux semblent pourtant faire ce qu’il faut. Des données récentes du CDC montrent que 90 % des hôpitaux américains ont cessé d’utiliser la colistine, a déclaré Martha Sharan, porte-parole de l’agence.
Les dirigeants du nombre décroissant de fabricants d’antibiotiques se plaignent que les programmes de gestion sont trop avares, au détriment des patients. Ils accusent en partie les programmes Medicare qui versent aux hôpitaux une somme forfaitaire pour le traitement d’une affection donnée. Un projet de loi du Congrès déposé en 2019 et soumis à nouveau l’année dernière exigerait que Medicare paie les nouveaux antibiotiques séparément. Les démocrates ont bloqué le projet de loi, mais les producteurs d’antibiotiques soutiennent que cela inciterait les hôpitaux à utiliser leurs médicaments.
Retenir les nouveaux antibiotiques permet à la résistance aux anciens médicaments de s’aggraver, et “cela rend de plus en plus difficile pour un nouvel antibiotique de faire son travail”, a déclaré Ted Schroeder, PDG du fabricant d’antibiotiques Nabriva et leader d’un groupe d’intérêt de l’industrie.
Mais l’essentiel est que la plupart des patients n’ont pas besoin des médicaments les plus récents, a déclaré M. Kadri.
Dans une étude NIH de 2020 que la FDA a aidé à financer, Kadri et ses collègues ont examiné les dossiers de 134 hôpitaux de 2009 à 2015 pour trouver des exemples de bactéries difficiles à traiter et hautement résistantes du type gram-négatif – un domaine clé de préoccupation. Sur environ 139 000 infections à Gram négatif, seules 1 352 entraient dans la catégorie des bactéries difficiles à traiter, soit environ 1 %.
“Il n’y a tout simplement pas assez de cas” pour créer un marché adéquat pour les nouveaux antibiotiques, a déclaré Kadri.
En extrapolant à partir de l’étude, le marché des nouveaux antibiotiques contre les bactéries gram-négatives hautement résistantes se situerait entre 120 et 430 millions de dollars par an, alors qu’il faut en moyenne 1 milliard de dollars pour développer un seul médicament, ont écrit les docteurs Neil Clancy et Minh-Hong Nguyen du Veterans Affairs Pittsburgh Healthcare System.
En l’absence d’un marché viable, les experts en maladies infectieuses, les sociétés pharmaceutiques et les groupes de patients se sont ralliés à la loi PASTEUR, introduite par le Sens. Michael Bennet (D-Colo.) et Todd Young (R-Ind.) l’année dernière. Ce projet de loi prévoit la création d’un fonds d’un montant maximal de 11 milliards de dollars sur 10 ans pour récompenser les antimicrobiens prometteurs qui sont sur le point d’être approuvés par la FDA ou qui l’ont été. Le gouvernement garantirait des paiements allant jusqu’à 3 milliards de dollars pour chaque médicament, éliminant ainsi l’incitation à la surconsommation.
PASTEUR a 40 co-sponsors au Sénat. Les experts pensent que son adoption est cruciale.
“Même si, sur la base de la population, le besoin de nouveaux médicaments est faible, vous ne voulez pas être ce patient” qui pourrait en avoir besoin, a déclaré Kadri. “Si vous l’êtes, vous voulez disposer d’un éventail de médicaments sûrs et efficaces.”
KHN (Kaiser Health News) est une salle de presse nationale qui produit un journalisme approfondi sur les questions de santé. Avec Policy Analysis and Polling, KHN est l’un des trois principaux programmes opérationnels de la KFF (Kaiser Family Foundation). La KFF est une organisation à but non lucratif qui fournit des informations sur les questions de santé à la nation.