La forte réponse en anticorps aux vaccins à ARNm a diminué au cours d’une période de suivi de huit mois ; La réponse initiale inférieure au vaccin Ad26 à injection unique est restée stable au fil du temps, selon la recherche.
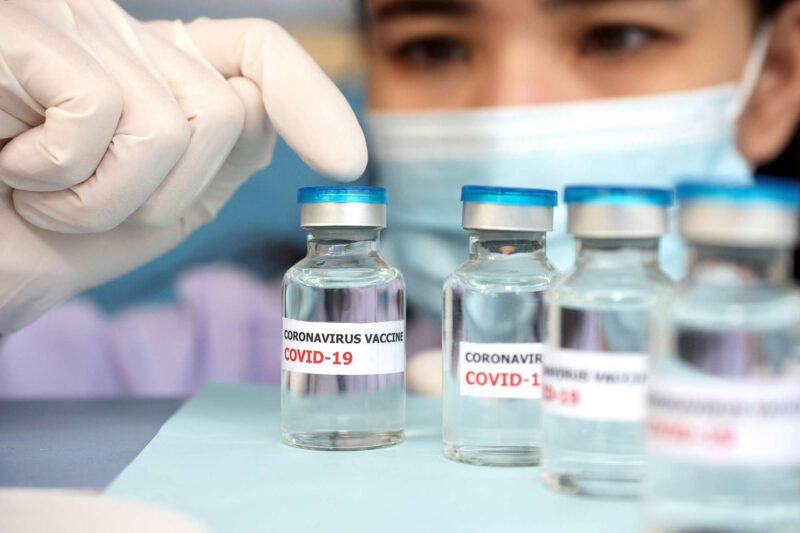
Sur la base de la solidité des données d’essais cliniques montrant que les vaccins conféraient une protection solide contre COVID-19[feminine, la Food & Drug Administration des États-Unis a accordé une autorisation d’utilisation d’urgence aux vaccins à base d’ARNm connus sous le nom de BNT162b2 (BioNTech, Pfizer) et mRNA-1273 (Moderna) en décembre 2020, et au single Ad26.COV2.S (Johnson & Johnson) -vaccin injecté en février 2021. À ce jour, près de 200 millions d’Américains ont reçu un vaccin COVID-19, et alors que certains approchent du premier anniversaire de leur vaccination, des questions subsistent sur l’efficacité à long terme des vaccins.
Dans un article publié dans le Journal de médecine de la Nouvelle-Angleterre, une équipe d’experts du Beth Israel Deaconess Medical Center (BIDMC) a comparé les réponses immunitaires induites par les trois vaccins sur une période de suivi de huit mois. Les chercheurs ont évalué les niveaux des 61 participants de divers anticorps, lymphocytes T et autres produits immunitaires deux à quatre semaines après l’immunisation complète – le moment du pic d’immunité – à huit mois après la vaccination. Trente et un participants ont reçu le vaccin BNT162b2, 22 ont reçu le vaccin à ARNm-1273 et huit ont reçu le vaccin Ad26.COV2.S.
« Les vaccins à ARNm étaient caractérisés par des pics élevés de réponses en anticorps qui ont fortement diminué au sixième mois et ont encore diminué au huitième mois », a déclaré l’auteur correspondant Dan H. Barouch, MD, PhD, directeur du Center for Virology and Vaccine Research au BIDMC, qui contribué au développement de la plateforme Ad26 en collaboration avec Johnson & Johnson. “Le vaccin Ad26 à injection unique a induit des réponses initiales en anticorps plus faibles, mais ces réponses étaient généralement stables dans le temps avec peu ou pas de signe de déclin.”
L’équipe a également découvert que l’ARNm-1273 provoquait des réponses d’anticorps qui étaient généralement plus élevées et plus durables que BNT162b2. Les trois vaccins ont démontré une large réactivité croisée avec des variantes de SRAS-CoV-2, le virus qui cause le COVID-19. Les résultats ont des implications importantes pour comprendre comment l’immunité vaccinale peut diminuer avec le temps ; Cependant, les réponses immunitaires précises nécessaires pour conférer une protection contre le SRAS-CoV-2 n’ont pas encore été déterminées, soulignent les chercheurs.
“Même si les niveaux d’anticorps neutralisants diminuent, des réponses stables des lymphocytes T et des fonctions d’anticorps non neutralisants à 8 mois peuvent expliquer comment les vaccins continuent d’offrir une protection solide contre le COVID-19 sévère”, a déclaré l’auteur principal Ai-ris Y. Collier, MD, spécialiste en médecine maternelle et fœtale au BIDMC. «Se faire vacciner (même pendant la grossesse) reste le meilleur outil dont nous disposons pour mettre fin à la pandémie de COVID-19.»
Référence : « Cinétique différentielle des réponses immunitaires provoquées par les vaccins Covid-19 » par Ai-ris Y. Collier, MD ; Jingyou Yu, Ph.D. ; Katherine McMahan, MS; Jinyan Liu, Ph.D. ; Abishek Chandrashekar, MS; Jenny S. Maron, BS; Caroline Atyeo, MS; David R. Martinez, Ph.D. ; Jessica L. Ansel, IP; Ricardo Aguayo, BS ; Marjorie Rowe, BS ; Catherine Jacob-Dolan, BS ; Daniel Sellers, BS ; Julia Barrett, BS ; Kunza Ahmad, MS ; Tochi Anioke, BS ; Haley VanWyk, BS ; Sarah Gardner, BS ; Pouvoirs d’Olivia, BS ; Esther A. Bondzie, BA; Huahua Wan, MS ; Ralph S. Baric, Ph.D. ; Galit Alter, Ph.D.; Michele R. Hacker, Sc.D. et Dan H. Barouch, MD, Ph.D., 15 octobre 2021, Journal de médecine de la Nouvelle-Angleterre.
DOI : 10.1056 / NEJMc2115596
Les co-auteurs comprenaient Jingyou Yu, PhD, Katherine McMahan, MS, Jinyan Liu, PhD, Abishek Chandrashekar, MS, Jessica L. Ansel, NP, Marjorie Rowe, BS, Ricardo Aguayo, BS, Catherine Jacob-Dolan, BS, Daniel Sellers , BS, Julia Barrett, BS, Kunza Ahmad, MS, Tochi Anioke, BS, Haley VanWyk, BS, Sarah Gardner, BS, Olivia Powers, BS, Esther A. Bondzie, BA, Huahua Wan, MS, et Michele R. Hacker , ScD de BIDMC; Jenny S. Maron, BS, Caroline Atyeo, MS et Galit Alter, PhD, du Ragon Institute of MGH, AVEC et Harvard ; et David R. Martinez, PhD, et Ralph S. Baric, PhD de l’Université de Caroline du Nord à Chapel Hill.
Les auteurs remercient Janssen Vaccines & Prevention, les National Institutes of Health (subvention CA26047), le Massachusetts Consortium for Pathogen Readiness, le Ragon Institute et la Musk Foundation. Les auteurs reconnaissent également le programme de développement des scientifiques de la reproduction pour le Eunice Kennedy Shriver National Institute of Child Health & Human Development et Burroughs Wellcome Fund (subvention HD000849), le Harvard Clinical and Translational Science Center (subvention TR0025410) et une bourse Hannah H. Gray. du Howard Hughes Medical Institute et un prix d’enrichissement postdoctoral du Burroughs Wellcome Fund.
Barouch est co-inventeur sur les brevets provisoires de vaccins (63/121, 482 ; 63/133, 969 ; 63/135, 182). Veuillez consulter le document pour une liste complète des divulgations.