Des scientifiques chinois ont récemment rapporté le rôle clé de la régulation de l’acétylation de l’histone dans la régulation des protéines non codantes longues. ARN appelé Régulateur de la mort cellulaire du lysosome (LCDR) dans la survie des tumeurs, ce qui constitue une cible diagnostique et thérapeutique potentielle pour le cancer du poumon.
Sous la direction du professeur GAO Shan, de l’Institut d’ingénierie et de technologie biomédicales de Suzhou de l’Académie chinoise des sciences (CAS), ces scientifiques ont révélé que l’élimination de la protéine LCDR dans la survie de la tumeur était un facteur important. LCDR dans les cellules cancéreuses du poumon pouvait favoriser l’apoptose. Les résultats ont été publiés dans PNAS.
Le lysosome est impliqué dans l’homéostasie cellulaire et sa dysrégulation a été liée à diverses maladies humaines, dont le cancer. Les LncRNA sont des ARN non codants d’une longueur supérieure à 200 nucléotides, dont la dérégulation est associée aux caractéristiques du cancer. Ils dirigent la croissance et la survie du cancer en interagissant avec les éléments suivants ADN l’ARN et les assemblages de protéines, y compris le système ribonucléique hétérogène. ribonucléique hétérogène(hnRNP), dont les fonctions sont l’épissage alternatif, la stabilité de l’ARN, la traduction, etc.
Cependant, la question de savoir si les lncRNA et/ou les hnRNP sont impliqués dans la survie du cancer médiée par le lysosome n’a pas été élucidée.
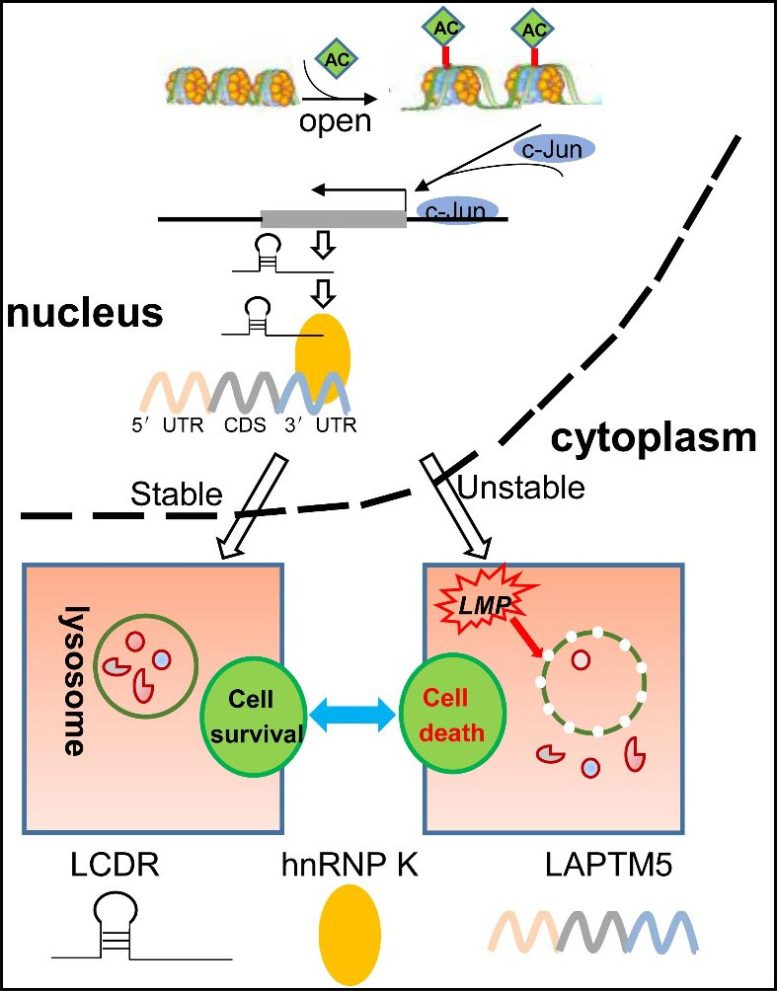
Modèle proposé pour l’axe LCDR/hnRNP K/LAPTM5 favorisant la pathogenèse du cancer du poumon. Crédit : GAO Shan
Dans cette étude, LCDR se lie à la ribonucléoprotéine nucléaire hétérogène K (hnRNP K) pour réguler la stabilité du transcrit de la protéine transmembranaire associée aux lysosomes (LAPTM5) qui maintient l’intégrité de la membrane lysosomale.
Selon les chercheurs, le knockdown de LCDR, hnRNP K ou LAPTM5 a favorisé la perméabilisation de la membrane lysosomale et la mort cellulaire lysosomale, entraînant ainsi l’apoptose. La surexpression de LAPTM5 ou l’inhibiteur de cathepsine B ont partiellement restauré les effets de cet axe sur la mort des cellules lysosomales. in vitro et in vivo.
De même, le ciblage LCDR a réduit de manière significative la croissance tumorale de xénogreffes d’adénocarcinome pulmonaire (LUAD) dérivées de patients et a entraîné une mort cellulaire significative en utilisant l’administration systématique de siRNA médiée par des nanoparticules (NPs).
De plus, LCDR/hnRNP K/LAPTM5 étaient régulés à la hausse dans les tissus de la LUAD, et leur co-expression a montré une valeur diagnostique accrue pour la LUAD.
Ces résultats mettent en lumière LCDR/hnRNP K/LAPTM5 comme cibles thérapeutiques potentielles et le ciblage des lysosomes est une stratégie prometteuse dans le traitement du cancer.
Référence : “LCDR Q:0 régule l’intégrité de la membrane lysosomale par le transcrit LAPTM5 stabilisé par hnRNP K et favorise la survie cellulaire” 17 janvier 2022,Actes de l’Académie nationale des sciences.
DOI : 10.1073/pnas.2110428119
Ce travail a été soutenu par la Fondation nationale des sciences naturelles de Chine et le projet pilote stratégique de science et technologie du CAS, etc.