Par
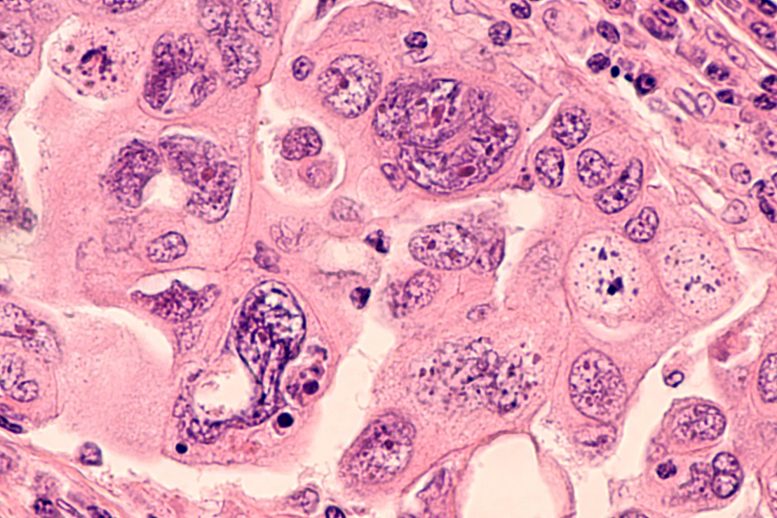
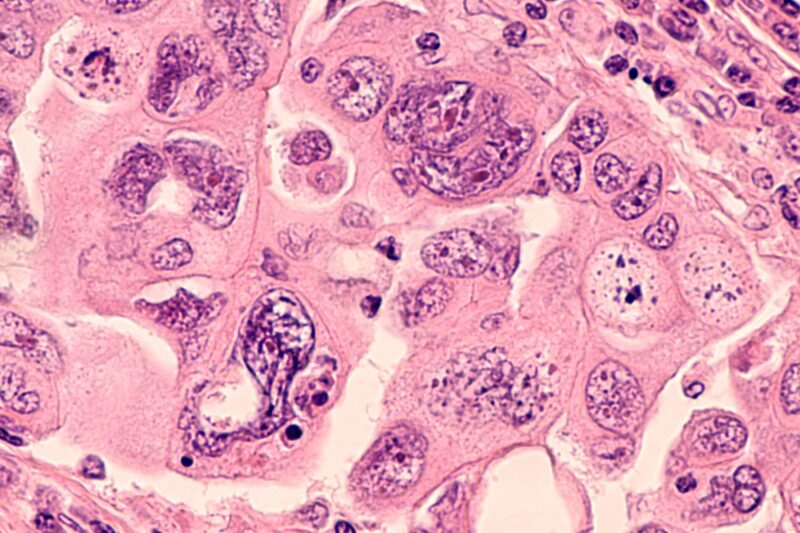
Image d’un carcinome séreux, la forme la plus maligne de cancer de l’ovaire.
La Food and Drug Administration des États-Unis a approuvé aujourd’hui Cytalux (pafolacianine), un médicament d’imagerie destiné à aider les chirurgiens à identifier les lésions cancéreuses de l’ovaire. Le médicament est conçu pour améliorer la capacité de localiser d’autres tissus cancéreux de l’ovaire qui sont normalement difficiles à détecter pendant la chirurgie.
Cytalux est indiqué chez les patientes adultes atteintes d’un cancer de l’ovaire pour aider à identifier les lésions cancéreuses pendant la chirurgie. Le médicament est un agent de diagnostic qui est administré sous la forme d’une injection intraveineuse avant la chirurgie.
« L’approbation de Cytalux par la FDA peut aider à améliorer la capacité des chirurgiens à identifier les tumeurs ovariennes mortelles qui pourraient autrement passer inaperçues », a déclaré Alex Gorovets, MD, directeur adjoint de l’Office of Specialty Medicine du Center for Drug Evaluation and Research de la FDA. « En complétant les méthodes actuelles de détection du cancer de l’ovaire pendant la chirurgie, Cytalux offre aux professionnels de santé une approche d’imagerie supplémentaire pour les patientes atteintes d’un cancer de l’ovaire.
L’American Cancer Society estime qu’il y aura plus de 21 000 nouveaux cas de cancer de l’ovaire et plus de 13 000 décès dus à cette maladie en 2021, ce qui en fait le plus meurtrier de tous les cancers de l’appareil reproducteur féminin. Le traitement conventionnel du cancer de l’ovaire comprend la chirurgie pour enlever autant de tumeurs que possible, la chimiothérapie pour arrêter la croissance des cellules malignes ou d’autres thérapies ciblées pour identifier et attaquer des cellules cancéreuses spécifiques.
Le cancer de l’ovaire amène souvent le corps à surproduire une protéine spécifique dans les membranes cellulaires appelée récepteur de folate. Après administration par injection, Cytalux se lie à ces protéines et s’illumine sous une lumière fluorescente, augmentant la capacité des chirurgiens à identifier le tissu cancéreux. Actuellement, les chirurgiens s’appuient sur l’imagerie préopératoire, l’inspection visuelle des tumeurs sous un éclairage normal ou l’examen au toucher pour identifier les lésions cancéreuses. Cytalux est utilisé avec un système d’imagerie par fluorescence proche infrarouge autorisé par la FDA pour une utilisation spécifique avec la pafolacianine.
L’innocuité et l’efficacité de Cytalux ont été évaluées dans une étude randomisée, multicentrique et ouverte portant sur des femmes diagnostiquées avec un cancer de l’ovaire ou avec une forte suspicion clinique de cancer de l’ovaire qui devaient subir une intervention chirurgicale. Sur les 134 femmes (âgées de 33 à 81 ans) qui ont reçu une dose de Cytalux et ont été évaluées à la fois sous lumière normale et fluorescente pendant la chirurgie, 26,9% ont eu au moins une lésion cancéreuse détectée qui n’a pas été observée par inspection visuelle ou tactile standard.
Les effets secondaires les plus courants de Cytalux étaient des réactions liées à la perfusion, notamment des nausées, des vomissements, des douleurs abdominales, des bouffées vasomotrices, une dyspepsie, une gêne thoracique, des démangeaisons et une hypersensibilité. Cytalux peut nuire au fœtus lorsqu’il est administré à une femme enceinte. L’utilisation de folate, folique acide, ou les suppléments contenant du folate doivent être évités dans les 48 heures précédant l’administration de Cytalux. Il existe un risque d’erreurs d’interprétation des images avec l’utilisation de Cytalux pour détecter le cancer de l’ovaire pendant la chirurgie, y compris les faux négatifs et les faux positifs.
La FDA a précédemment accordé à Cytalux les désignations de médicament orphelin, prioritaire et accéléré.
La FDA a accordé l’approbation à On Target Laboratories, LLC.