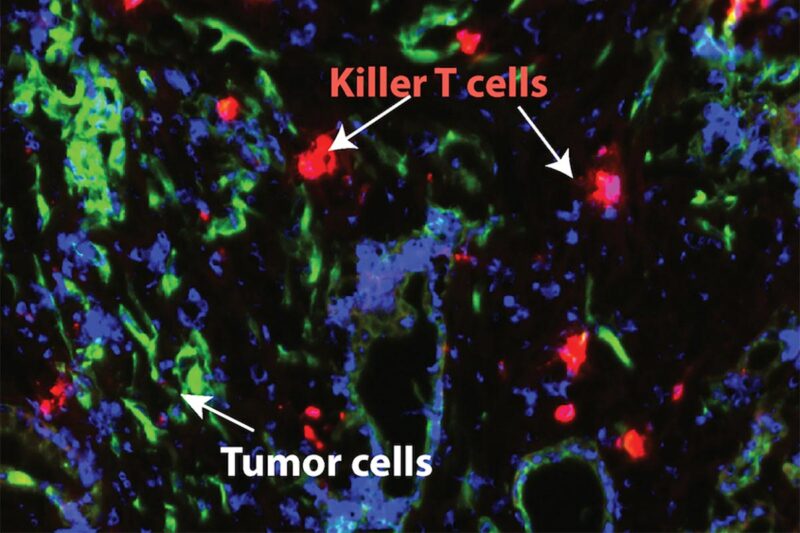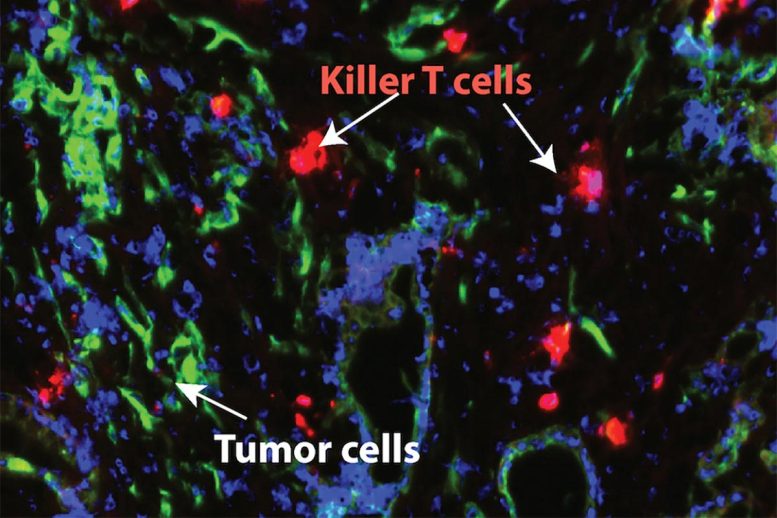
De nouvelles recherches menées par la faculté de médecine de l’université Washington à St. Louis montrent que le blocage d’une voie inflammatoire majeure dans le cancer du pancréas rend les tumeurs sensibles à la chimiothérapie et à un type d’immunothérapie qui aide les cellules T du système immunitaire à attaquer les cellules cancéreuses. Ci-dessus, les cellules cancéreuses du pancréas sont représentées en vert. Les cellules T sont en rouge. Crédit : LIM LAB
L’Université de Washington va diriger un essai clinique national sur une thérapie.
Le cancer du pancréas est l’un des types de tumeurs les plus agressifs et les plus mortels. Il est connu pour sa résistance à pratiquement tous les types de traitement, y compris les nouvelles immunothérapies.
Louis, suggère que le blocage d’une voie inflammatoire majeure activée dans le cancer du pancréas rend les tumeurs sensibles à la chimiothérapie et à un type d’immunothérapie qui incite les cellules T du système immunitaire à attaquer les cellules cancéreuses. La thérapie a plus que doublé la survie dans un modèle murin de cancer du pancréas.
Les résultats de l’étude, publiés aujourd’hui (7 mars 2022) dans le journal Gastroenterologyapportent un soutien supplémentaire à la justification d’un nouvel essai clinique national qui évaluera la même stratégie de traitement chez les patients atteints d’adénocarcinome du canal pancréatique, la tumeur maligne la plus courante du pancréas. Les chercheurs prévoient de recruter environ 50 patients dans tout le pays.
Les chercheurs de l’université de Washington, du Siteman Cancer Center de l’hôpital Barnes-Jewish et de l’école de médecine de l’université de Washington, dirigeront l’essai national qui fait partie du réseau d’essais cliniques des thérapies expérimentales de l’Institut national du cancer (NCI), une collaboration entre l’industrie, les centres médicaux universitaires et les chercheurs qui se concentrent sur les premières études cliniques des thérapies innovantes contre le cancer. Le réseau comprend plus de 30 sites cliniques aux États-Unis et au Canada.
“L’Université de Washington possède de nombreux atouts pour faire passer la science du laboratoire à la clinique”, a déclaré l’auteur principal, Kian-Huat Lim, MD, PhD, professeur associé de médecine et chercheur principal pour la science translationnelle de l’essai national. “Avec cette thérapie, nous nous attaquons à une voie que nous savons être impliquée dans l’agressivité du cancer du pancréas. Les résultats de cette étude sont prometteurs dans la mesure où ils ont montré un moyen de percer les défenses de ce type de tumeur, la rendant sensible à nos thérapeutiques, y compris les combinaisons de chimiothérapie et les nouvelles immunothérapies qui stimulent les cellules T pour combattre le cancer.”
Les chercheurs, dont le premier auteur Vikas Somani, PhD, associé de recherche postdoctoral dans le laboratoire de Lim, dans la division d’oncologie du département de médecine, ont découvert qu’une protéine appelée IRAK4 dirige l’inflammation dans les tumeurs pancréatiques et conduit à l’épuisement des cellules T, ce qui signifie que les cellules T ne peuvent pas fonctionner comme elles le devraient pour attaquer les cellules nocives, y compris le cancer. Les chercheurs ont testé un inhibiteur d’IRAK4, appelé CA-4948, et ont constaté que le traitement réduisait la signalisation inflammatoire dans les tumeurs chez les souris et améliorait la capacité des cellules T à infiltrer les tumeurs et à tuer les cellules cancéreuses du pancréas. Le traitement a également sensibilisé les tumeurs à un type d’immunothérapie appelé immunothérapie à points de contrôle, qui “freine” les cellules T, améliorant ainsi leur capacité à attaquer les cellules tumorales.
Les chercheurs ont découvert que l’inhibiteur IRAK4 bloque une voie clé appelée NF-kappaB, connue depuis longtemps pour son rôle dans le développement du cancer. De nombreuses recherches se concentrent sur la neutralisation de cette voie et de ses effets en aval après son activation. Un élément nouveau de cette thérapie est que l’inhibiteur d’IRAK4 empêche l’activation de la voie nocive en premier lieu.
Chez des souris présentant un modèle agressif commun de cancer du pancréas, les chercheurs ont constaté que l’inhibiteur d’IRAK4 seul augmentait la survie par rapport à un placebo ou à une chimiothérapie. En association, l’inhibiteur d’IRAK4 et la chimiothérapie augmentaient encore la survie par rapport au placebo ou à la chimiothérapie seule. De plus, lorsqu’il était associé à deux immunothérapies, l’inhibiteur d’IRAK4 prolongeait significativement la survie, passant d’une moyenne de 25 jours avec l’inhibiteur seul à une moyenne de 46 jours avec l’association inhibiteur plus immunothérapie. Certaines des souris ont survécu jusqu’à 100 jours avec la thérapie combinée.
L’inhibiteur d’IRAK4 fait déjà l’objet d’essais cliniques nationaux visant à étudier son utilisation contre les cancers du sang.
“Nous sommes impatients de commencer l’essai clinique national de ce médicament chez les patients atteints de cancer du pancréas – l’essai est une étape directe de la recherche sur le cancer du sang.La traduction de cet article particulier”, a déclaré Haeseong Park, MD, professeur associé de médecine et chercheur principal du nouvel essai. “Nous sommes ravis de travailler avec le NCI et les sites cliniques du réseau d’essais cliniques sur les thérapies expérimentales afin de pouvoir exploiter notre science innovante locale et la porter au niveau national.”
Bientôt, l’équipe de Park commencera également un essai monocentrique au Siteman Cancer Center pour tester la sécurité et l’efficacité de l’inhibiteur IRAK4 CA-4948 dans le cancer gastrique.
Référence : “IRAK4 signaling drives resistance to checkpoint immunotherapy in pancreatic ductal adenocarcinoma” par Somani VK, et al, 7 mars 2022, Gastroentérologie.
Ce travail a été soutenu par les National Institutes of Health (NIH), numéros de subvention R37CA219697-01 et 1P50CA196510-01A1 ; l’American Cancer Society, numéro de subvention RSG- 17-203-01-TBG ; le Washington University Specialized Program of Research Excellence (SPORE) in Pancreatic Cancer Career Enhancement Award, numéro de subvention 1P50CA196510-01A1 ; et le Alvin J. Siteman Cancer Center Siteman Investment Program, qui est soutenu par le Barnard Trust et The Foundation for Barnes-Jewish Hospital.
La société de biotechnologie CURIS a fourni l’inhibiteur d’IRAK4, CA-4948, utilisé dans cette étude.