Des chercheurs de l’Université de Californie, à San Francisco, ont réussi à tirer parti d’un médicament approuvé par la FDA pour arrêter la croissance de tumeurs dues à des mutations du gène RAS, qui sont réputées difficiles à traiter et sont responsables d’environ un décès par cancer sur quatre.
Profitant de ce qu’ils ont découvert comme étant l’appétit des cellules cancéreuses pour une forme réactive de fer, les chercheurs ont modifié un médicament anticancéreux pour qu’il n’agisse que dans ces cellules riches en fer, laissant les autres cellules fonctionner normalement. Cette réussite, décrite dans le numéro du 9 mars 2022 du Journal of Experimental Medicine pourrait ouvrir la voie à une chimiothérapie plus tolérable pour de nombreux cancers pour lesquels les traitements actuels peuvent être aussi difficiles que la maladie.
“Les mutations RAS, à elles seules, causent plus de misère que tous les autres cancers réunis, et prennent tant de vies dans le monde”, a déclaré Eric Collisson, MD, auteur principal de l’étude et membre du UCSF Helen Diller Family Comprehensive Cancer Center. “Cette étude nous rapproche considérablement de la réponse au besoin non satisfait d’un meilleur traitement de ces cancers.”
Un médicament contre le cancer avec un capteur de fer
Pour ce faire, Collisson et l’auteur principal Honglin Jiang, MD, tous deux oncologues à l’UCSF, ont fait équipe avec Adam Renslo, PhD, chimiste pharmaceutique également à l’UCSF et co-auteur principal, pour se concentrer sur les cancers pancréatiques et gastro-intestinaux mutés par le gène RAS. Le gène RAS joue un rôle dans le contrôle des voies de la cellule qui l’incitent à croître et à se diviser. Les mutations de ce gène signifient généralement que ces forces de croissance ne sont pas contrôlées, ce qui conduit au cancer.
Les traitements actuels, comme le cobimétinib, parviennent à bloquer cette activité de croissance excessive déclenchée par la mutation, mais ils le font également dans de nombreux autres tissus non cancéreux, ce qui entraîne des effets secondaires graves que de nombreux patients jugent intolérables.
“Le cobimétinib est un exemple classique de médicament anticancéreux dont nous savons qu’il fonctionne bien sur sa cible, mais qui n’a pas atteint son potentiel clinique parce que la même cible est importante dans la peau et d’autres tissus normaux”, a déclaré M. Renslo.
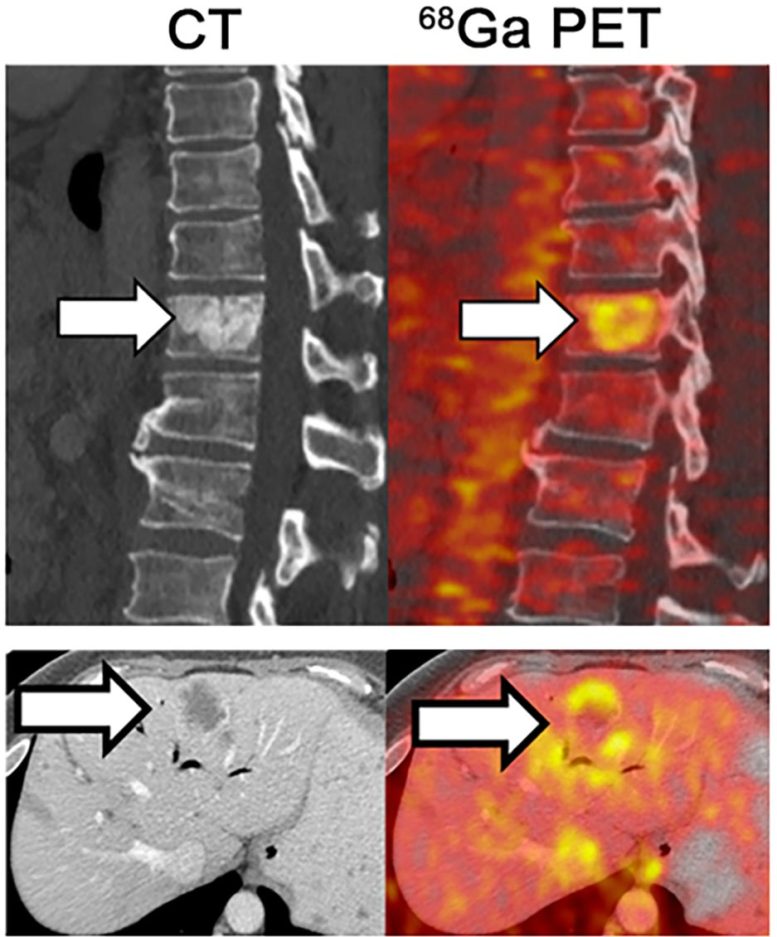
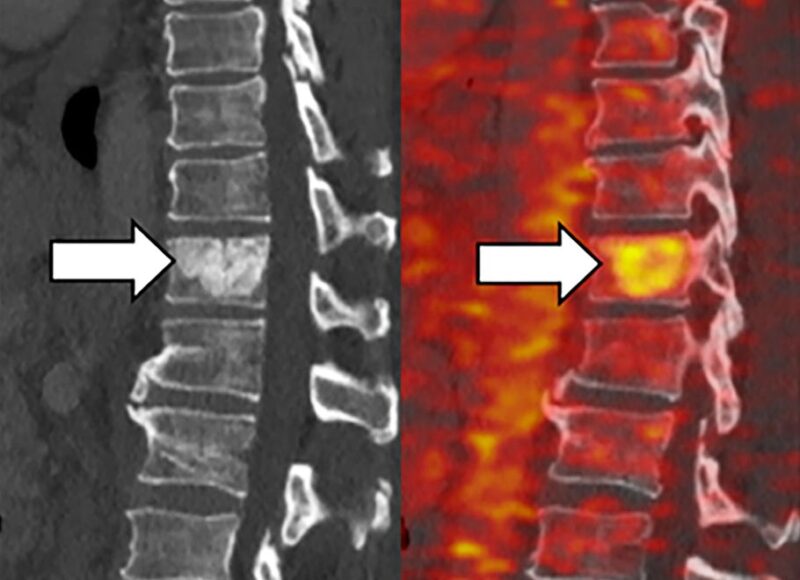
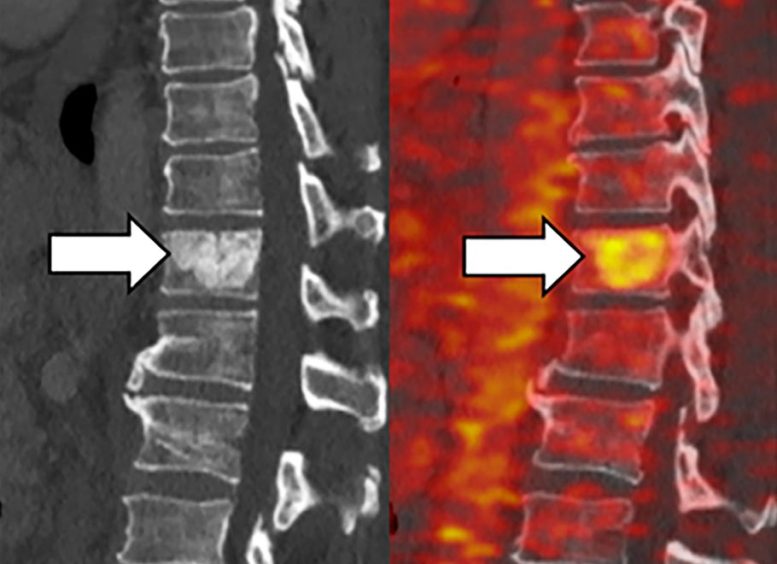
L’imagerie TEP (à droite) montre l’accumulation de fer dans les tumeurs métastatiques se développant dans la colonne vertébrale et le foie de patients atteints d’adénocarcinome canalaire pancréatique. Crédit : 2022 Jiang et al. Publié à l’origine dans le Journal of Experimental Medicine. https://doi.org/10.1084/jem.20210739
Les chercheurs ont découvert que de nombreuses tumeurs induites par la forme KRAS des mutations RAS présentent des concentrations élevées de fer ferreux – une forme de l’élément qui est très réactive – et que cela est corrélé à des durées de survie plus courtes.
Pour tirer parti de cette caractéristique unique des cellules cancéreuses, Renslo et Ryan Muir, alors étudiant diplômé, ont synthétisé une nouvelle version du cobimetinib portant un petit capteur moléculaire de fer ferreux. Le capteur désactive effectivement le cobimetinib jusqu’à ce qu’il rencontre du fer ferreux dans les cellules cancéreuses.
Après avoir confirmé que le nouveau médicament, baptisé TRX-cobimetinib, évitait les effets indésirables sur les tissus normaux comme la peau qui limitent le dosage chez les patients humains, les chercheurs ont testé le composé dans des modèles murins de plusieurs cancers induits par le KRAS et ont constaté qu’il était tout aussi efficace que le cobimetinib pour réduire les tumeurs.
Permettre de nouvelles combinaisons de médicaments
La toxicité réduite a permis aux chercheurs de combiner le TRX-cobimetinib avec d’autres médicaments anticancéreux synergiques pour fournir des traitements combinés qui se sont avérés encore plus efficaces pour inhiber la croissance des tumeurs et ont été mieux tolérés que les combinaisons comparables utilisant le cobimetinib.
“En éliminant la toxicité de l’équation, on ne parle pas seulement d’un nouveau médicament, mais de 10 nouvelles combinaisons que l’on peut maintenant envisager d’explorer en clinique”, a déclaré Renslo. “Ce serait le home run de cette approche”.
Renslo est déjà au travail pour étudier si une approche similaire peut être appliquée aux antibiotiques, dont certains ont des effets secondaires fâcheux, pour cibler le traitement et réduire la toxicité.
M. Collisson, qui travaille tous les jours avec des patients atteints de ces cancers, a déclaré que la collaboration avec M. Renslo lui a donné l’espoir de pouvoir offrir à ces patients de meilleures options dans un avenir pas trop lointain. Et, a-t-il ajouté, cette expérience lui a ouvert les yeux sur des choses qu’il avait manquées en étant si concentré sur son univers oncologique quotidien.
“J’adore m’occuper des patients, et une partie fondamentale de cette tâche consiste, en fin de compte, à acheminer une molécule là où elle est nécessaire et à l’éloigner des endroits où elle ne l’est pas”, a-t-il déclaré. “Pour être capable de délivrer unUne thérapie cinq fois plus puissante que celle dont nous disposons actuellement et qui n’épuise pas le patient, c’est plutôt excitant.”
Référence : “Un conjugué médicamenteux activable par le fer ferreux réalise un blocage puissant de MAPK dans les tumeurs pilotées par KRAS” 9 mars 2022, Journal of Experimental Medicine.
DOI : 10.1084/jem.20210739
Les autres auteurs de l’étude sont Ryan Gonciarz, Adam Olshen, Iwei Yeh, Byron Hann, Ning Zhao, Yung-hua Wang, Spencer Behr et Michael Evans, tous de l’UCSF, et James Korkola, de l’Université de la santé et des sciences de l’Oregon.
Ce travail a été soutenu par les subventions NIH, NCI CA178015, CA222862, CA227807, CA239604, CA230263, CA210974, CA224081, P30CA082103, AI105106, W81XWH1810763, et W81XWH1810754. Voir l’étude pour un financement supplémentaire.