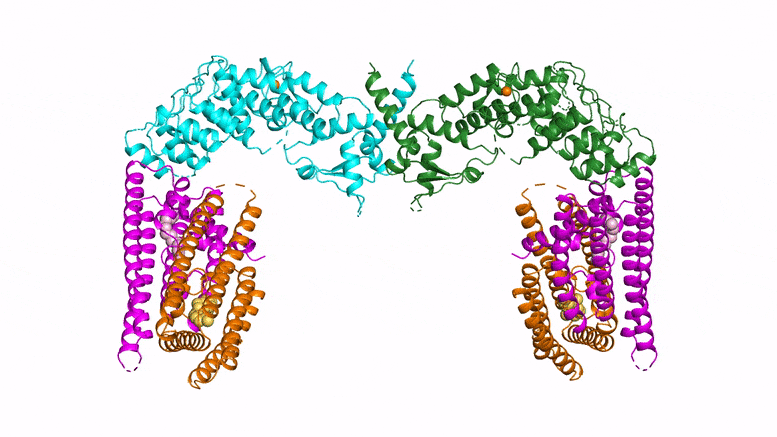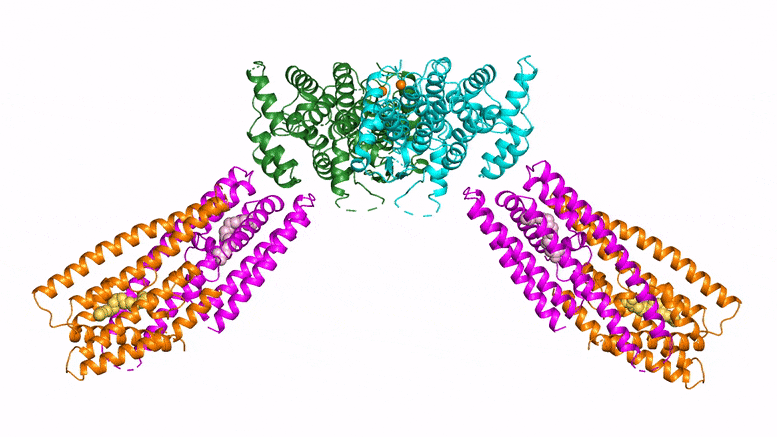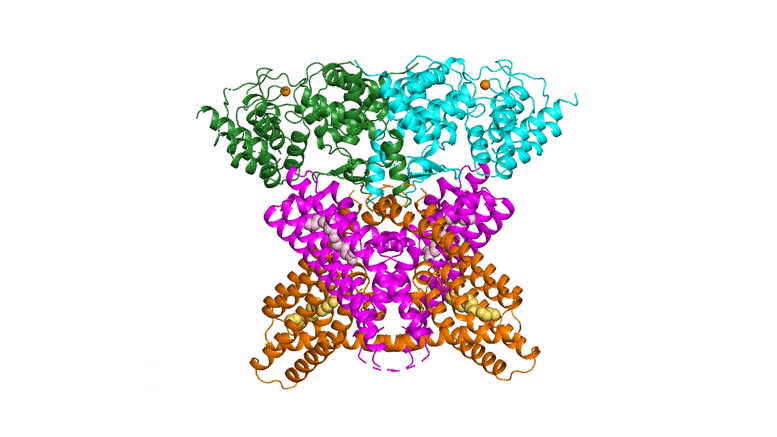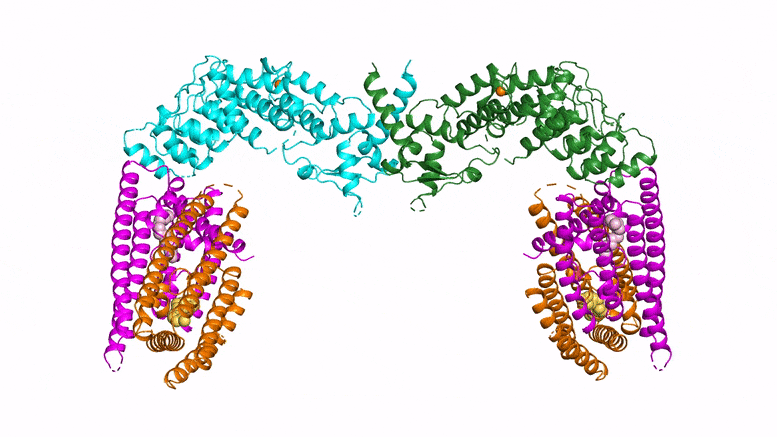
Les chercheurs ont utilisé deux techniques d’imagerie et de cristallographie pour découvrir la structure d’une protéine clé de défense des plantes appelée NPR1, qui ressemble à un “oiseau planeur”. Crédit : Xinnian Dong/HHMI/Université de Duke
La biologiste Xinnian Dong dit que son “meilleur cadeau de Noël” est arrivé sous la forme d’un appel téléphonique. Il s’agissait d’un appel de son ami de longue date et collaborateur à l’Université Duke, Pei Zhou, qui lui annonçait la nouvelle tant attendue : ils avaient enfin résolu la structure de la protéine de défense des plantes NPR1.
Dong, un chercheur de l’Institut médical Howard Hughes, a découvert la NPR1. il y a vingt-cinq ans. Cette protéine, dont le nom est inspiré par l’amour de Dong pour la National Public Radio (NPR), joue un rôle important dans la protection des plantes à fleurs contre un large éventail d’agents pathogènes. Aujourd’hui, NPR1 est largement reconnue comme un régulateur principal qui contrôle plus de 2 000 gènes impliqués dans l’immunité des plantes.
Malgré son rôle important dans la défense des plantes, la structure de NPR1 est restée insaisissable, au grand dam des chercheurs dans ce domaine. Sans données détaillées sur la structure, les scientifiques ont eu du mal à comprendre comment la protéine régit la protection des plantes, explique Zhou. “Ce qui est vraiment crucial et manquant, c’est une explication du fonctionnement de la NPR1 au niveau moléculaire.”

Lorsqu’elle est exposée à des agents pathogènes, la plante de laboratoire commune A. thaliana s’appuie sur une protéine de défense appelée NPR1 pour rester en bonne santé (à droite). Les plantes dépourvues de NPR1 (à gauche) sont infectées et développent des feuilles jaunes. Crédit : Raul Zavaliev/Duke University
Dans de nouveaux travaux qui dévoilent l’apparence et l’action de NPR1, les équipes de Zhou et de Dong comblent cette lacune – une découverte qui pourrait changer la face de la sélection végétale. Les deux groupes rapportent la structure de NPR1 de la plante de laboratoire commune. Arabidopsis thaliana aujourd’hui (11 mai 2022) dans la revue Nature.
Pour Mme Dong, cet article marque la fin d’une quête longue de plusieurs décennies. “Lorsque j’ai vu pour la première fois la structure de NPR1, j’en ai eu le souffle coupé”, dit-elle. “Elle ressemblait à un oiseau planant, tout simplement magnifique”.
Des plantes en pleine forme
Depuis que l’homme cultive des plantes, il doit lutter contre les nombreux parasites et agents pathogènes qui entravent leur croissance. La moisissure de l’eau Phytophthora infestansresponsable de la famine de la pomme de terre en Irlande, qui a fait un million de morts et deux millions de réfugiés. “C’est une lutte énorme qui a façonné notre monde”, déclare M. Dong.
Aujourd’hui, les agents pathogènes continuent de s’attaquer aux bananes, aux avocats et à d’autres cultures populaires. Mais s’attaquer au problème avec des approches traditionnelles peut s’avérer problématique. Les pesticides chimiques, par exemple, sont souvent toxiques pour l’environnement. C’est l’une des raisons pour lesquelles les phytogénéticiens se tournent désormais vers des solutions génétiques, comme l’ingénierie des cellules végétales pour produire des niveaux élevés de NPR1. Cette approche s’est avérée efficace en laboratoire et dans des essais limités sur le terrain, mais avec un hic : plus l’immunité augmente, plus la croissance diminue.
Les chercheurs ont utilisé deux techniques d’imagerie et de cristallographie pour découvrir la structure d’une protéine clé de défense des plantes appelée NPR1, qui ressemble à “un oiseau qui plane”. Crédit : Xinnian Dong/HHMI/Université de Duke
Les nouvelles connaissances sur la structure et le comportement de la NPR1 pourraient aider les chercheurs à contourner ce problème et à concevoir de meilleures cultures, explique Jonathan Jones, biologiste végétal au Sainsbury Laboratory de Norwich, au Royaume-Uni, qui n’a pas participé à cette recherche. “Comprendre comment la protéine fonctionne et interagit avec d’autres molécules pourrait être très utile pour améliorer la résistance des plantes aux maladies”, ajoute-t-il.
Un oiseau aux ailes déployées
Zhou, Dong et leurs collègues ont résolu la structure de NPR1 en utilisant la cristallographie aux rayons X et la technique d’imagerie par cryo-microscopie électronique (cryo-EM). De nombreux laboratoires ont essayé et échoué au fil des ans, explique Jijie Chai, biologiste structurel à l’université de Cologne, qui n’a pas participé à ces travaux. “La NPR1 est notoirement difficile à purifier pour l’imagerie”, explique-t-il.
Le succès de l’équipe est dû à l’utilisation complémentaire des deux techniques. La cryo-EM a permis aux chercheurs d’obtenir une structure préliminaire de la NPR1, ce qui leur a donné un aperçu crucial de la manière de préparer la protéine pour une cristallographie réussie. Le résultat : des images à haute résolution de la NPR1 et de ses régions fonctionnelles clés.
Si des études antérieures ont permis d’entrevoir certaines parties de la structure de la protéine NPR1, aucune n’était “aussi complète que celle présentée dans ce nouvel article”, déclare Jones. Les nouvelles imagesrévèlent que deux protéines NPR1 s’assemblent, formant une structure qui ressemble à un oiseau aux ailes déployées. À l’extrémité des ailes, NPR1 se lie à des molécules situées dans le noyau de la cellule pour activer les gènes immunitaires des plantes, a découvert l’équipe de Dong. “Quatre années d’expérimentation ont valu la peine d’attendre”, dit-elle.
Maintenant, son équipe veut découvrir comment la protéine NPR1 prend une nouvelle forme lorsqu’une infection la met en action. “Cette étude a permis non seulement de répondre à de nombreuses questions de longue date, mais aussi d’ouvrir de nouvelles voies de recherche”, déclare Mme Dong. “C’est une période passionnante”.
Référence : “Base structurelle de NPR1 dans l’activation de l’immunité des plantes” 11 mai 2022, Nature.
DOI: 10.1038/s41586-022-04699-w


