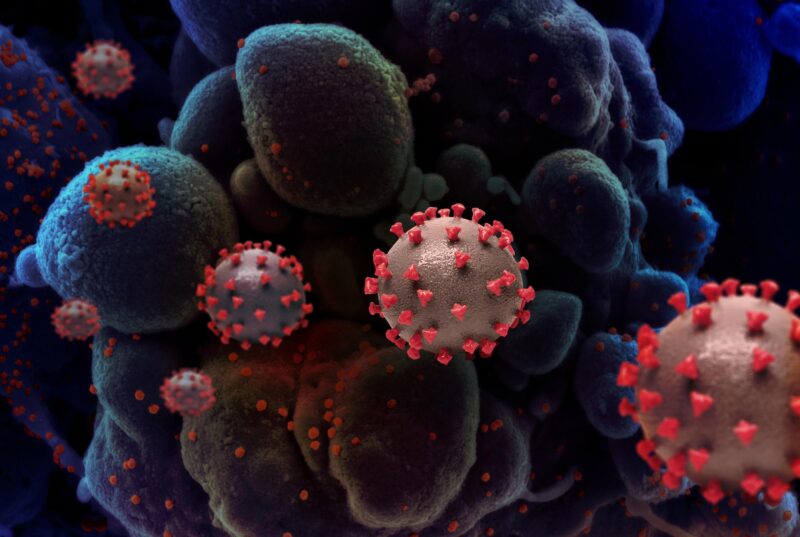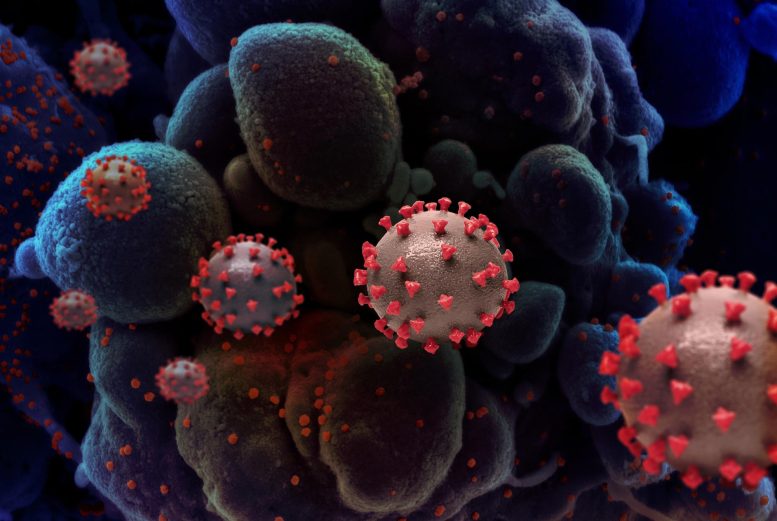
Crédit : Institut national des allergies et des maladies infectieuses, NIH
Des chercheurs du UArizona College of Medicine – Tucson ont découvert que le lysat bactérien OM-85 bloquait SRAS-CoV-2 infection en diminuant la capacité du coronavirus à se lier au récepteur de surface des cellules pulmonaires ACE2.
Une équipe de chercheurs en sciences de la santé de l’Université de l’Arizona au UArizona College of Medicine – Tucson a découvert qu’une combinaison d’extraits bactériens utilisés en Europe pour traiter les infections respiratoires peut offrir un nouveau moyen de prévenir ou de réduire l’infection par le SRAS-CoV-2, le virus ça cause COVID-19[feminine.
L’étude, publiée dans le Journal d’allergie et d’immunologie clinique, a montré qu’une combinaison spécifique d’extraits bactériens connue sous le nom d’OM-85 inhibait l’infection par le SRAS-CoV-2 en réduisant la capacité du virus à se fixer aux cellules pulmonaires. L’OM-85 est un lysat bactérien, une combinaison de molécules extraites des parois cellulaires des bactéries, commercialisé hors des États-Unis sous la marque Broncho-Vaxom comme traitement préventif des infections des voies respiratoires supérieures chez les enfants et les adultes.
« Les stratégies actuelles de prévention des infections reposent sur des vaccins qui déclenchent une réponse de notre système immunitaire principalement en produisant des anticorps. Les anticorps se fixent à une partie spécifique du virus qui agit comme la clé et l’empêchent de pouvoir se fixer au récepteur des cellules pulmonaires, qui est comme un verrou à l’extérieur de la cellule pulmonaire. Cette étude est unique car c’est la première fois que des chercheurs ciblent le récepteur – le verrou – avec un extrait bactérien et montrent qu’il protège contre l’infection par un virus vivant. Nous retirons essentiellement le verrou de la paroi cellulaire afin qu’il n’y ait rien à quoi s’attacher la clé du virus », a déclaré l’auteur principal, le Dr Donata Vercelli, professeur de médecine cellulaire et moléculaire à l’UArizona College of Medicine – Tucson et professeur de génétique. à l’Institut BIO5.
Lorsque le SRAS-CoV-2 pénètre dans les poumons, il se lie à des récepteurs, notamment le récepteur de l’enzyme de conversion de l’angiotensine 2, connu sous le nom d’ACE2, sur les membranes externes des cellules pulmonaires. Une enzyme cellulaire modifie la forme d’une protéine sur le virus pour permettre au SRAS-CoV-2 de franchir la membrane et d’infecter la cellule.
Lorsque la pandémie a commencé, Vercelli et Vadim Pivniouk, professeur agrégé au Département de médecine cellulaire et moléculaire, ainsi que d’autres membres de l’équipe de recherche, se sont tournés vers les données qu’ils ont recueillies dans une étude de prévention de l’asthme pour déterminer si le traitement à l’OM-85 affectait l’ACE2 récepteur et enzyme impliqués dans COVID-19.
Vercelli a collaboré avec le Dr Janko Nikolich-Žugich, professeur et président du Département d’immunobiologie et membre de BIO5, et Jennifer Uhrlaub, chercheur associé, et a découvert que le prétraitement des cellules avec OM-85 empêchait l’infection par le SRAS-CoV-2. La capacité de l’OM-85 à prévenir l’infection virale s’est avérée dépendante de sa capacité à diminuer l’expression du récepteur ACE2.
“ACE2 est l’élément essentiel qui fait pencher la balance”, a déclaré Vercelli, qui est également directeur de la génomique moléculaire au Centre de recherche sur l’asthme et les voies respiratoires. “Sans cette pièce jointe initiale – la clé s’insérant dans une serrure – l’ensemble du processus infectieux est déraillé et bloqué.”
Le mécanisme par lequel OM-85 prévient l’infection virale est différent de celui des vaccins ou des traitements par anticorps, qui se concentrent sur une protéine virale. En ciblant le récepteur, l’OM-85 peut fermer la porte même qui permet au coronavirus d’infecter les cellules, ce qui pourrait le rendre efficace contre toutes les variantes qui infectent les cellules via le récepteur ACE2.
“Des études originales de ce type nous obligent à tester si l’infection par le virus vivant peut être bloquée par le traitement préventif potentiel en question”, a déclaré Nikolich-Žugich. « Cela doit être fait dans des installations de confinement de biosécurité spécialisées, donc notre longue expérience avec ce type de travail et notre installation de biosécurité à BIO5 nous ont permis d’aider le Dr Vercelli et son équipe dans cette étude. »
Vercelli et Pivniouk ont également fait appel à la Dre Monica Kraft, titulaire de la chaire Robert et Irene Flinn du Collège de médecine de Tucson, qui a collecté des cellules pulmonaires primaires de patients en bonne santé.
La justification de l’utilisation d’extraits bactériens pour prévenir l’infection virale est liée à une étude précédente dirigée par Vercelli, qui est également le directeur du Centre de l’Arizona pour la biologie des maladies complexes. En 2016, son équipe a découvert que l’exposition à des produits microbiens environnementaux a protégé les enfants des fermes amish de l’asthme et des allergies.
“Notre système immunitaire inné a évolué sous des pressions environnementales telles que les bactéries, mais nos modes de vie actuels ne nous donnent souvent pas la chance de développer cette immunité protectrice”, a déclaré Vercelli. “Notre idée est d’utiliser un lysat bactérien pour entraîner notre système immunitaire à nous protéger des virus, de la même manière que ceux qui sont régulièrement exposés aux animaux de ferme sont protégés contre une multitude de bactéries et autres microbes.”
Selon Vercelli, le traitement avec des lysats bactériens tels que l’OM-85 pourrait favoriser un échange plus interactif entre le système immunitaire et les microbes.
Référence : « Le lysat bactérien OM-85 inhibe l’infection par le SARS-CoV-2 des cellules épithéliales en régulant à la baisse l’expression du récepteur SARS-CoV-2 » par Vadim Pivniouk, PhD ; Oksana Pivniouk, MA ; Avery DeVries, PhD; Jennifer L. Uhrlaub, MS ; Ashley Michael, BS ; Denis Pivniouk, BS; Sydney R. VanLinden, BS; Michelle Y. Conway, BS ; Seongmin Hahn, MS ; Sean P. Malone; Paix Ezeh, PhD; Jared M. Churko, PhD; Dayna Anderson, BS ; Monica Kraft, MD; Janko Nikolich-Zugich, MD, PhD et Donata Vercelli, MD, 9 décembre 2021, Journal d’allergie et d’immunologie clinique.
DOI : 10.1016 / j.jaci.2021.11.019
Cette recherche a été financée en partie par OM Pharma SA, et par le National Institutes of Health’s National Institute of Environmental Health Sciences (T32ES007091), National Heart, Lung and Blood Institute (T32 HL007249, R25HL126140) et National Institute of Allergy and Infectious Diseases (P01AI148104, R21AI144722).