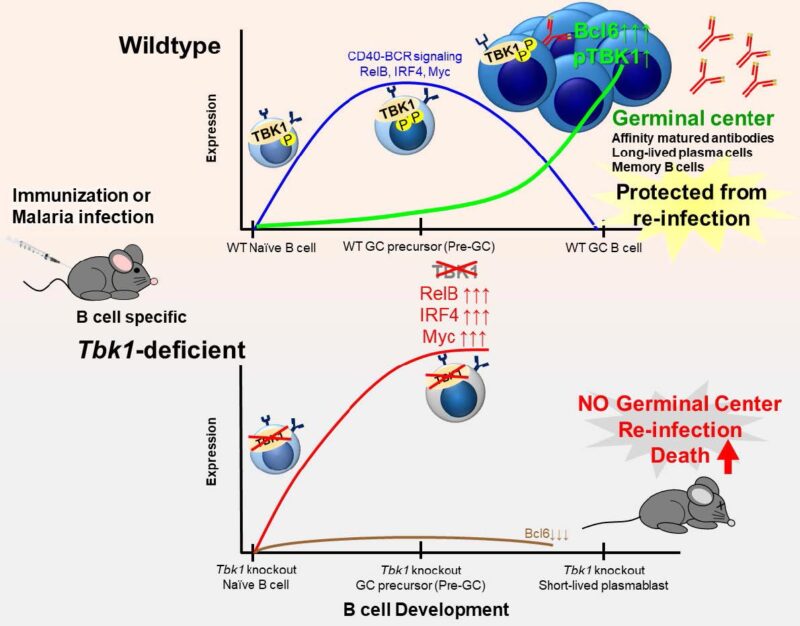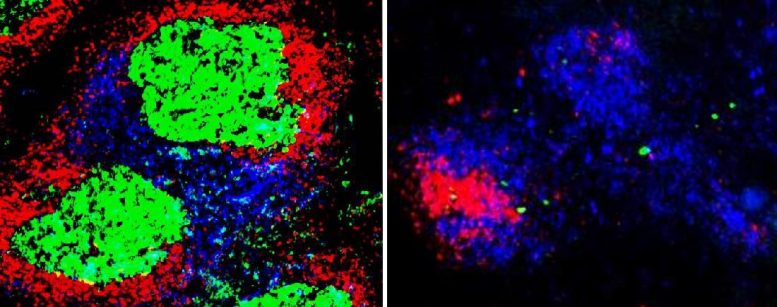
Avec un système immunitaire sain, l’infection amène les cellules T folliculaires CD4+ (bleues) et les cellules B immatures (rouges), deux types de globules blancs, à former une structure temporaire appelée centre germinatif (vert) dans les organes du système immunitaire. Des cellules spléniques prélevées sur une souris saine (à gauche) et une souris génétiquement modifiée pour ne contenir l’enzyme TBK1 que dans les cellules B (à droite) montrent que TBK1 est essentiel à la formation normale du centre germinatif lors d’une infection palustre. Crédit : Image de Michelle SJ Lee (CC BY-ND)
Une étude sur la souris identifie l’enzyme intrinsèque TBK1 comme essentielle pour déterminer le destin des cellules B.
Des experts japonais ont identifié une partie fondamentale de la mémoire à long terme du système immunitaire, fournissant un nouveau détail utile dans la poursuite de la conception de meilleurs vaccins contre des maladies, allant de COVID-19[feminine au paludisme. La recherche, publiée dans le Journal de médecine expérimentale, révèle un nouveau rôle pour l’enzyme TBK1 dans la détermination du sort des cellules B mémoire du système immunitaire.
Le système immunitaire est composé de nombreux types de cellules, mais les deux types pertinents pour ce projet de recherche de l’Université de Tokyo sont les globules blancs appelés lymphocytes T auxiliaires folliculaires CD4+ et lymphocytes B. Une fois que le corps a reconnu une infection, les cellules T auxiliaires folliculaires libèrent des signaux chimiques qui amènent les cellules B immatures à apprendre et à se souvenir des agents pathogènes à attaquer. Ce processus de signalisation des cellules T à B et d’entraînement des cellules B se produit au sein d’une structure cellulaire temporaire appelée centre germinatif dans les organes du système immunitaire, y compris la rate, les ganglions lymphatiques et les amygdales. Les cellules B mémoire développées au sein du centre germinatif mémorisent un agent pathogène la première fois qu’il vous infecte, puis si jamais il pénètre à nouveau dans votre corps, les cellules B mémoire matures et entraînées l’attaquent en induisant la production d’anticorps avant que l’agent pathogène ne puisse se multiplier, vous épargnant ainsi se sentir malade une deuxième fois.
« L’un des objectifs de la vaccination est de produire des cellules B mémoire de haute qualité pour une production d’anticorps de longue durée », a déclaré la professeure adjointe de projet Michelle SJ Lee de l’UTokyo Institute of Medical Science, premier auteur de la récente publication.
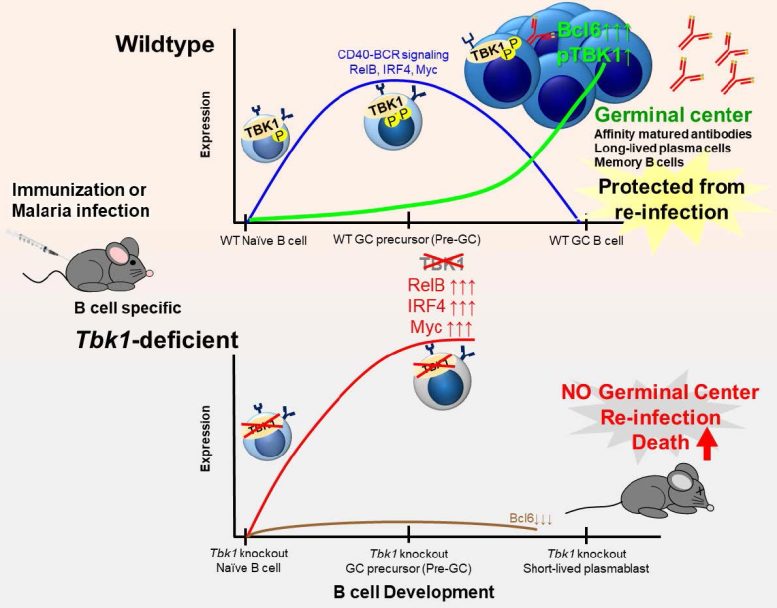
L’activité normale de l’enzyme TBK1 dans un type de globules blancs appelés cellules B est essentielle à la formation de la mémoire à long terme dans le système immunitaire. Les chercheurs d’UTokyo ont travaillé avec des souris saines (type sauvage, moitié supérieure de l’image) et des souris génétiquement modifiées pour ne manquer de TBK1 que dans leurs cellules B (déficientes en TBK1, moitié inférieure de l’image). Lorsque des souris saines ont été infectées par le parasite du paludisme transmis par les moustiques, TBK1 réduit l’activité des gènes qui bloquent le développement des cellules B, leur permettant de se développer en cellules B mémoire matures. Les cellules B des souris déficientes en TBK1 restent immatures, ce qui signifie que si les souris survivent à leur première infection palustre, leur système immunitaire ne conserve aucune mémoire à long terme du parasite et est extrêmement vulnérable à une infection palustre répétée. Crédit : Image de Michelle SJ Lee (CC BY-ND)
« Il y a de nombreux facteurs à prendre en compte lors de la conception de vaccins pour une immunité de longue durée, nous ne devons donc pas nous concentrer uniquement sur le seul centre germinatif. Mais si vous n’avez pas de centre germinatif fonctionnel, vous serez alors très sensible à la réinfection », a déclaré Lee.
Cependant, il n’y a pas de limite au nombre de fois où vous pouvez être piqué par des moustiques et réinfecté par le parasite du paludisme. D’une manière ou d’une autre, les parasites du paludisme échappent aux cellules B mémoire. Bien que les enfants soient plus susceptibles de mourir du paludisme que les adultes, certaines personnes peuvent tomber gravement malades malgré un certain nombre d’infections paludéennes antérieures.
Cette capacité du parasite à prévenir et à échapper aux cellules B efficaces est ce qui fait du paludisme un agent pathogène intéressant pour le professeur Cevayir Coban, qui dirige la division d’immunologie du paludisme à l’UTokyo Institute of Medical Science et est le dernier auteur du document de recherche avec Lee et ses collaborateurs. à l’Université d’Osaka.
« Nous voulons comprendre les principes fondamentaux de la réponse immunitaire naturelle. Quoi que nous fassions, nous devrions viser à bénéficier à terme aux patients atteints de paludisme », a déclaré Coban. “La pandémie de COVID-19 a attiré l’attention mondiale sur les maladies infectieuses et l’intérêt pour la conception de vaccins, nous avons donc une chance de renouveler l’attention sur les maladies négligées comme le paludisme”, a-t-elle poursuivi.
Depuis de nombreuses années, la communauté scientifique a identifié un large éventail de rôles pour la molécule TBK1, une enzyme qui peut altérer l’activité de gènes ou d’autres protéines en ajoutant des marqueurs chimiques, grâce à un processus appelé phosphorylation. TBK1 a des rôles bien connus dans l’immunité antivirale. Cependant, aucun groupe de recherche n’avait connecté TBK1 au destin des cellules B et au centre germinatif.
Les chercheurs ont génétiquement modifié des souris qui avaient des gènes TBK1 non fonctionnels uniquement dans des types de cellules spécifiques, principalement des cellules B ou des cellules T CD4+. Ce knock-out spécifique au type de cellule de TBK1 donne aux chercheurs une idée plus claire de ce qu’un gène avec de nombreux travaux fait dans différentes cellules du corps. Coban, Lee et leurs collègues ont infecté ces souris modifiées et des souris adultes saines avec le parasite du paludisme, ont observé leur santé, puis ont examiné des échantillons de leur rate et de leurs ganglions lymphatiques.
Les images microscopiques ont révélé que les centres germinatifs ne se forment que chez les souris qui ont TBK1 fonctionnel dans leurs cellules B. Les souris sans TBK1 dans leurs cellules B étaient plus susceptibles de mourir et de mourir plus tôt de l’infection palustre que leurs pairs normaux. Des expériences supplémentaires ont montré que les quelques souris qui ont survécu au paludisme sans TBK1 dans leurs cellules B étaient capables d’utiliser d’autres types de réponses immunitaires, mais elles peuvent être réinfectées.
Cependant, la suppression de TBK1 uniquement des cellules T auxiliaires folliculaires CD4+ n’a eu aucun effet sur les centres germinatifs ou sur la façon dont les souris ont souffert d’une infection paludéenne.
Une analyse plus poussée a confirmé que sans TBK1, de nombreuses protéines dans les cellules B immatures présentaient une phosphorylation anormale par rapport aux cellules B immatures normales. Pour différents gènes, une phosphorylation anormale peut provoquer des augmentations ou des diminutions anormales de l’activité. Les chercheurs soupçonnent que dans les cellules B, l’activité TBK1 agit comme un interrupteur pour certains gènes, désactivant essentiellement les gènes qui piègent les cellules B dans leur état immature.
“C’est la première fois que l’on montre que TBK1 est essentiel dans les cellules B pour former les centres germinatifs et produire des anticorps matures de haute qualité”, a déclaré Lee.
Les chercheurs espèrent qu’avec des connaissances plus fondamentales sur les mystères restants du système immunitaire, les futurs vaccins pourront être conçus pour produire une immunité plus durable, potentiellement sans avoir besoin de plusieurs doses de vaccin. Cependant, la conception d’un vaccin sera toujours compliquée par les qualités uniques de chaque agent pathogène et de ses versions mutées, en particulier dans le cas d’agents pathogènes à évolution rapide comme le Sars-CoV-2, le virus à l’origine du COVID-19.
“Pour l’instant, nous pouvons au moins dire qu’un vaccin efficace conçu pour produire une immunité protectrice de longue durée ne devrait pas réduire l’activité de TBK1 dans les cellules B”, a déclaré Coban.
Référence : “B cell intrinsèque TBK1 is essential for germinal center formation during infection and vaccination in mouse” par Michelle SJ Lee, Takeshi Inoue, Wataru Ise, Julia Matsuo-Dapaah, James B. Wing, Burcu Temizoz, Kouji Kobiyama, Tomoya Hayashi, Ashwini Patil, Shimon Sakaguchi, A. Katharina Simon, Jelena S. Bezbradica, Satoru Nagatoishi, Kouhei Tsumoto, Jun-Ichiro Inoue, Shizuo Akira, Tomohiro Kurosaki, Ken J. Ishii et Cevayir Coban, 15 décembre 2021, Journal de médecine expérimentale.
DOI : 10.1084 / jem.20211336