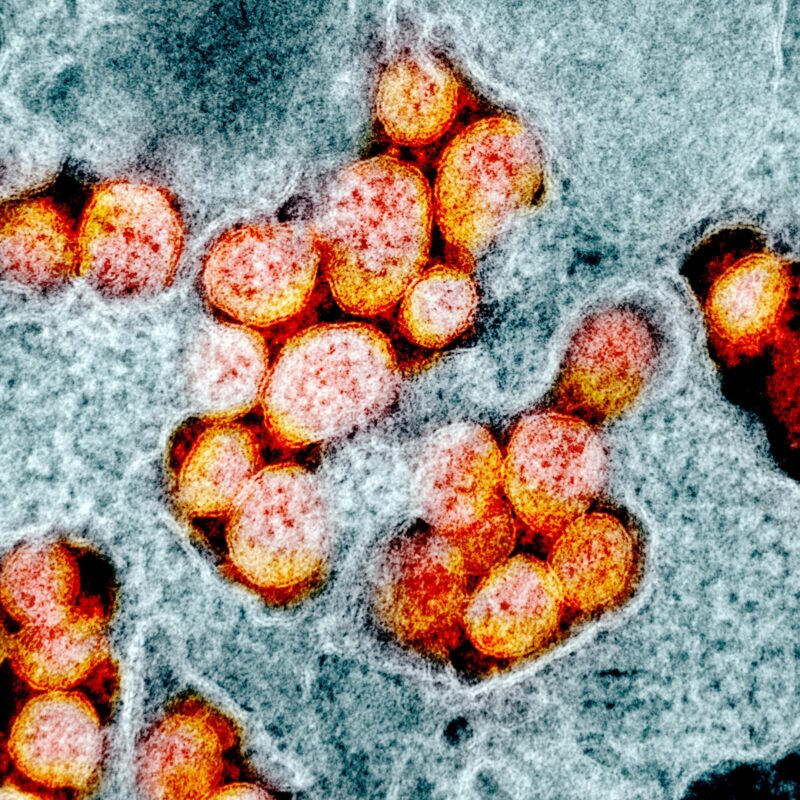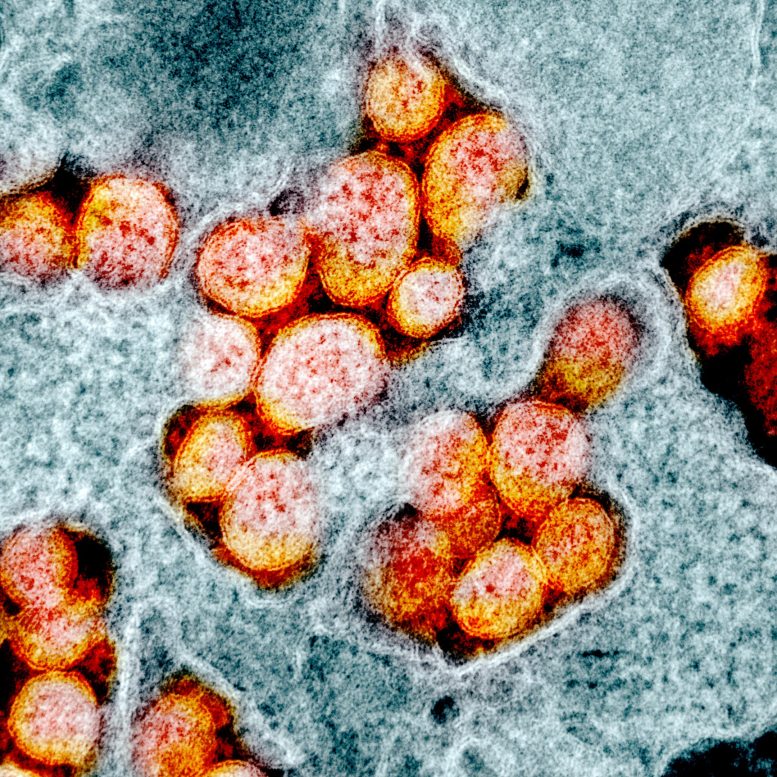
Les virus pénètrent dans les cellules pour en faire des copies et provoquer une infection. L’un des secrets du succès du SRAS-CoV-2 est de se cacher du système immunitaire en se propageant entre les cellules. Cette micrographie électronique à transmission montre des particules virales causant le COVID qui ont été isolées d’un patient. Crédit : National Institute of Allergy and Infectious Diseases, NIH.
Une étude met en lumière la transmissibilité du virus COVID et sa résistance à l’immunité de l’hôte.
Le virus qui cause COVID-19 a adopté des stratégies furtives pour rester en vie, et l’un des secrets de son succès est de se cacher du système immunitaire en se propageant par transmission de cellule à cellule, selon une nouvelle étude.
Des expériences de culture cellulaire ont montré que SRAS-CoV-2qui est à l’origine de la COVID-19, limite la libération de particules virales qui peuvent être inactivées par les anticorps, et qu’il reste plutôt replié dans les parois cellulaires et se propage entre les cellules.
“Il s’agit essentiellement d’une forme souterraine de transmission”, a déclaré l’auteur principal, Shan-Lu Liu, professeur de virologie au département des biosciences vétérinaires de l’université d’État de l’Ohio et chercheur au centre de recherche sur les rétrovirus de l’université.
“Le SRAS-CoV-2 peut se propager efficacement d’une cellule à l’autre parce qu’il n’existe pratiquement aucun obstacle à l’immunité de l’hôte. Les cellules cibles deviennent des cellules donneuses, et cela devient simplement une vague de propagation, car le virus peut ne pas sortir des cellules.”
Liu et ses collègues ont trouvé d’autres détails révélateurs sur le SRAS-CoV-2 : la protéine spike à sa surface permet à elle seule la transmission de cellule à cellule, et pourtant le récepteur primaire du virus sur les cellules cibles – auquel la spike se lie – n’est pas un élément nécessaire à l’opération de transmission de cellule à cellule. En outre, ils ont constaté que les anticorps neutralisants sont moins efficaces contre le virus lorsqu’il se propage dans les cellules.
Cette recherche a été publiée récemment dans le journal Proceedings of the National Academy of Sciences.
L’un des principaux points de cette étude consistait à comparer le SRAS-CoV-2 au coronavirus à l’origine de l’épidémie de SRAS de 2003, connu sous le nom de SRAS-CoV. Les résultats aident à expliquer pourquoi, alors que la première épidémie a entraîné des taux de mortalité beaucoup plus élevés et n’a duré que huit mois, nous sommes sur le point de dépasser les deux ans de la pandémie actuelle, avec une majorité de cas asymptomatiques, a déclaré Liu.
La comparaison a montré que le CoV-SRAS à l’origine du SRAS en 2003 est plus efficace que le CoV-SRAS-2 pour ce que l’on appelle la transmission acellulaire, lorsque des particules virales flottant librement infectent des cellules cibles en se liant à un récepteur à leur surface – mais restent également vulnérables aux anticorps produits par une infection antérieure et aux vaccins. Le SRAS-CoV-2, en revanche, est plus efficace dans la transmission de cellule à cellule, ce qui le rend plus difficile à neutraliser par les anticorps.
Les différences d’efficacité des virus ont été démontrées pour la première fois lors d’expériences utilisant des pseudovirus – un noyau viral non infectieux décoré à la surface par les deux types de protéines de pointe du coronavirus.
“La protéine de pointe est nécessaire et suffisante pour la transmission intercellulaire du SRAS-CoV-2 et du SRAS-CoV, car la seule différence entre ces pseudovirus était les protéines de pointe “, a déclaré Liu, également directeur du programme sur les virus et les pathogènes émergents de l’Institut des maladies infectieuses de l’Ohio.
En examinant de plus près ces différences, les chercheurs ont découvert que le SRAS-CoV-2 est également plus capable que le SRAS-CoV d’initier la fusion avec la membrane d’une cellule cible, une autre étape clé du processus d’entrée du virus. Et cette action de fusion plus forte a été associée à l’amélioration de la transmission intercellulaire du virus.
Paradoxalement, Liu a également découvert qu’une fusion trop importante de la membrane cellulaire entraînait la mort des cellules et pouvait en fait interférer avec la transmission de cellule à cellule.
L’équipe s’est ensuite penchée sur le rôle du récepteur ACE2, une protéine présente sur les surfaces cellulaires qui sert de porte d’entrée au virus responsable du COVID-19. Les chercheurs ont découvert, de manière inattendue, que les cellules dont la surface est dépourvue d’ACE2 ou qui en contiennent peu peuvent être pénétrées par le virus, ce qui permet une transmission robuste de cellule à cellule.
“Il n’y a pas de corrélation parfaite entre l’infection par le SRAS-CoV-2 et le niveau d’ACE2”, a déclaré Liu. “L’ACE2 peut être nécessaire pour l’infection initiale, mais une fois l’infection établie, le virus peut ne plus avoir besoin d’ACE2 car il peut se propager de cellule à cellule.”
Enfin, lors d’expériences consistant à comparer des échantillons de sang provenant de patients humains atteints de COVID-19 au virus authentique du SRAS-CoV-2, les chercheurs ont déterminé que le virus pouvait échapper à la réponse des anticorps en se propageant de cellule à cellule.mais que la neutralisation du virus par les anticorps dans le mode de transmission acellulaire était efficace.
“Nous avons pu confirmer que la transmission de cellule à cellule n’est pas sensible à l’inhibition par les anticorps des patients COVID ou des individus vaccinés”, a déclaré Liu. “La résistance de la transmission de cellule à cellule à la neutralisation par les anticorps est probablement quelque chose que nous devrions surveiller car des variantes du SRAS-CoV-2 continuent d’apparaître, y compris la plus récente, Omicron. En ce sens, le développement de médicaments antiviraux efficaces ciblant d’autres étapes de l’infection virale est essentiel.”
De nombreuses inconnues subsistent, notamment le mécanisme exact utilisé par le virus pour se propager d’une cellule à l’autre, la manière dont cela peut influencer les réponses des individus à l’infection virale, et si une transmission efficace d’une cellule à l’autre contribue ou non à l’émergence et à la propagation de nouveaux variants. Le laboratoire de Liu prévoit d’autres études utilisant le virus authentique et des cellules pulmonaires humaines pour approfondir ces questions.
Référence : “SARS-CoV-2 spreads through cell-to-cell transmission” par Cong Zeng, John P. Evans, Tiffany King, Yi-Min Zheng, Eugene M. Oltz, Sean P. J. Whelan, Linda J. Saif, Mark E. Peeples et Shan-Lu Liu, 22 décembre 2021, Actes de l’Académie nationale des sciences.
DOI : 10.1073/pnas.2111400119
Ce travail a été soutenu par des subventions des National Institutes of Health et des fonds provenant d’un donateur privé anonyme à Ohio State.
Les co-auteurs de l’Ohio State sont Cong Zeng, Jack Evans, Tiffany King, Yi-Min Zheng, Eugene Oltz, Linda Saif et Mark Peeples, également chercheur au Nationwide Children’s Hospital. Sean Whelan, de l’école de médecine de l’université de Washington, a également apporté sa contribution.