Une équipe de recherche de l’Université d’Okayama au Japon a prédit théoriquement une nouvelle classe de phases de glace, appelées aeroices, probablement les phases solides les plus stables de l’eau près de la température du zéro absolu sous pression négative.
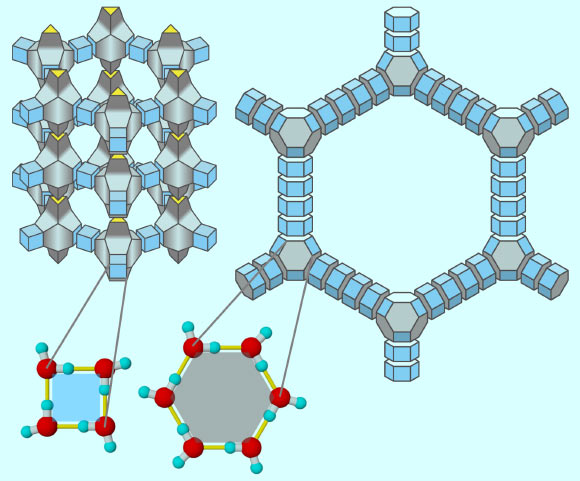
La glace zéolitique (à gauche) et l’aéroglace (à droite) sont illustrées : leur structure peut être considérée comme une combinaison de quelques blocs de construction polyédriques. À l’échelle moléculaire, chaque face polygonale des polyèdres est constituée de molécules d’eau (en bas à gauche) ; les lignes jaunes représentent les liaisons hydrogène. Crédit image : Masakazu Matsumoto / CC BY 2.0.
L’eau possède de nombreuses phases de glace qui se forment dans différentes conditions de pression et de température. Les effets d’une pression positive ont été largement explorés et les résultats sont assez prévisibles : plus la pression augmente, plus la densité de la glace augmente.
On en sait beaucoup moins, cependant, sur les effets d’une pression négative extrême sur les molécules d’eau.
En explorant une région importante de pression négative par le biais de simulations de dynamique moléculaire, Masakazu Matsumoto, chercheur à l’Université d’Okayama, et ses co-auteurs ont maintenant prédit théoriquement une nouvelle classe de phases de glace – les aérogels.
“Notre recherche, qui étudie pour la première fois une région entière de pression négative, constitue une étape importante dans l’exploration de ce territoire vaste et complexe du diagramme de phase”, a déclaré M. Matsumoto.
“On a également découvert que les glaces dont la densité est inférieure à celle de la glace normale sont multiples”.
Dix-sept phases de glace ont été trouvées expérimentalement, chacune étant numérotée dans l’ordre de sa découverte.
En 2014, le Dr Werner Kuhs de l’Université de Göttingen et ses coauteurs ont découvert une phase de glace qui se forme sous pression négative : la glace XVI.
Les molécules de la glace forment une structure zéolitique, une cage cristalline en 3D, dans laquelle des molécules ou des atomes invités sont piégés. Les molécules invitées (des particules de néon dans ce cas) ont été retirées, ce qui a permis d’obtenir une glace stable de très faible densité à des pressions négatives élevées.
En utilisant une technique similaire, une équipe dirigée par Xiao Cheng Zeng de l’Université de Nebraska-Lincoln et Jijun Zhao de l’Université de technologie de Dalian a découvert la glace XVII en 2016.
Matsumoto et ses collègues ont cartographié toutes les phases de glace possibles qu’il pourrait encore rester à explorer dans la région de pression négative.
Sachant que la structure de la silice (SiO2) et la glace sont communes, les chercheurs ont récupéré 200 zéolites de silice dans la base de données des zéolites.
Ils ont réarrangé les atomes dans les zéolithes SiO2 en retirant les deux atomes d’oxygène et en remplaçant l’atome de silicium de chaque molécule par un atome d’oxygène. Ensuite, les atomes d’hydrogène ont été ajoutés pour que la structure obéisse à la règle de la glace.
Dans la gamme de densité qui n’est qu’environ la moitié de celle de l’eau liquide (0.5 g/cm3), l’équipe a montré que la phase de glace nouvellement découverte est plus stable que n’importe quelle glace zéolite étudiée jusqu’à présent.
Les auteurs ont également simulé des structures de glace encore moins dense (0-0.5 g/cm3) en ajoutant des blocs de construction polyédriques aux structures zéolitiques pour rendre la structure plus éparse tout en satisfaisant à la règle structurelle de la glace.
La recherche est publiée dans le Journal of Chemical Physics.