En utilisant des techniques de rayonnement synchrotron à haute pression au Brookhaven National Laboratory (BNL), une équipe de chercheurs a examiné la structure, la liaison et les propriétés électroniques de l’hydrogène hautement comprimé connu sous le nom de phase IV de l’hydrogène.
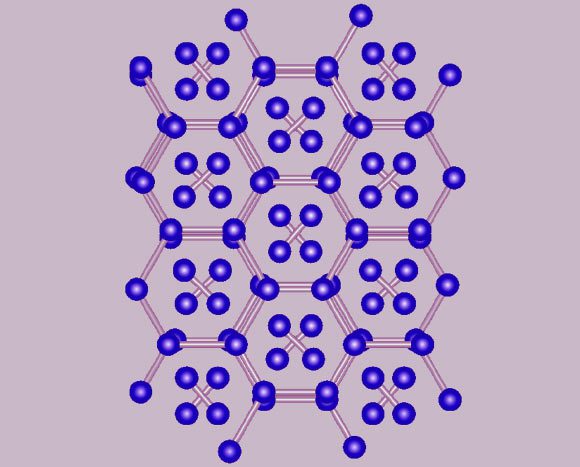
Structure de type graphène de la phase IV de l’hydrogène (Université d’Edimbourg)
Dans des conditions normales, l’hydrogène est un gaz composé de molécules diatomiques. Les molécules d’hydrogène commencent à changer lorsque la pression augmente. Ces différentes formes sont appelées phases et l’hydrogène a trois phases solides connues.
La phase I de l’hydrogène est un cristal quantique constitué de molécules d’hydrogène en rotation sur un réseau hexagonal très compact.
Les phases moléculaires II et III, ordonnées en fonction de leur orientation, apparaissent respectivement à environ 1,1 et 1,5 million de fois la pression atmosphérique normale.
La phase IV de l’hydrogène solide dense a été découverte en 2012 par une équipe de scientifiques des États-Unis et du Royaume-Uni.
Dans la nouvelle étude, le Dr Russell Hemley du Laboratoire de géophysique du BNL et ses collègues ont constaté que la phase IV était stable d’environ 2,2 millions de fois la pression atmosphérique normale et environ 80 degrés Fahrenheit à au moins 3,4 millions de fois la pression atmosphérique et environ moins 100 degrés Fahrenheit.
Leurs expériences ont révélé que l’hydrogène prend dans ces conditions une forme qui diffère remarquablement de ses autres structures connues.
La phase IV comporte deux types très différents de molécules d’hydrogène dans sa structure. Un premier type de molécules interagit très faiblement avec ses molécules voisines, ce qui est inhabituel pour des molécules soumises à ce type de compression très élevée. L’autre type de molécule se lie à ses voisines, formant des feuilles planes surprenantes.
Les mesures montrent également que l’hydrogène solide, dans ces conditions, se situe à la limite entre un semi-conducteur, comme le silicium, et un semi-métal, comme le graphite.
Ces résultats réfutent les affirmations précédentes selon lesquelles l’hydrogène forme un métal atomique dense à ces pressions et températures.
Cet élément simple – avec seulement un électron et un proton – continue de nous surprendre par sa richesse et sa complexité lorsqu’il est soumis à des pressions élevées”, a déclaré le Dr Hemley, qui est l’auteur principal d’un article publié dans le magazine “The News”. Physical Review Letters.
“Les résultats fournissent un important terrain d’essai pour la théorie fondamentale”, a déclaré le Dr Hemley.


