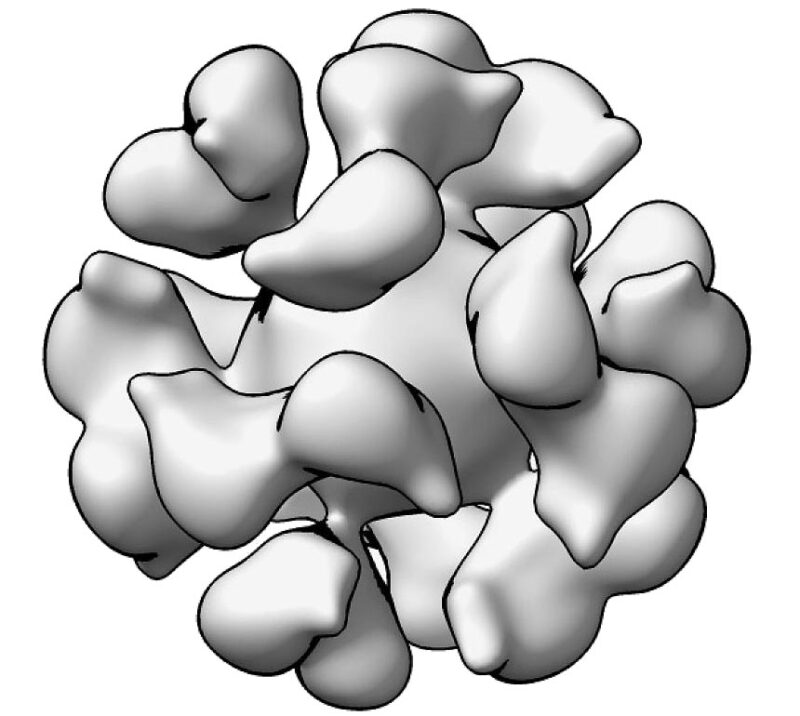
Modèle de reconstruction par microscopie cryoélectronique de la nanoparticule gp350-ferritine du virus d’Epstein-Barr. Crédit : Geng Meng, Université de Purdue.
L’Institut national des allergies et des maladies infectieuses (NIAID), qui fait partie des Instituts nationaux de la santé (NIH), a lancé un essai clinique de stade précoce pour évaluer un vaccin préventif expérimental contre le virus d’Epstein-Barr (EBV). L’EBV est la principale cause de la mononucléose infectieuse (“mono”) et est associé à certains cancers et maladies auto-immunes. L’étude de phase 1 est l’une des deux seules études à tester un vaccin expérimental contre l’EBV depuis plus de dix ans. Elle sera menée au NIH Clinical Center à Bethesda, Maryland.
L’EBV est un membre de la famille des virus de l’herpès et l’un des virus humains les plus courants. Il se propage par les fluides corporels, notamment la salive. Aux États-Unis, on estime à 125 000 le nombre de cas de mononucléose infectieuse chaque année ; environ 10 % de ces personnes développent une fatigue qui dure six mois ou plus. Environ 1 % de toutes les personnes infectées par l’EBV développent des complications graves, notamment une hépatite, des problèmes neurologiques ou de graves anomalies sanguines. L’EBV est également associé à plusieurs tumeurs malignes, notamment les cancers de l’estomac et du nasopharynx et les lymphomes de Hodgkin et de Burkitt, ainsi qu’à des maladies auto-immunes, comme le lupus érythémateux disséminé et la sclérose en plaques.
“Un vaccin qui pourrait prévenir ou réduire la gravité de l’infection par le virus d’Epstein-Barr pourrait réduire l’incidence de la mononucléose infectieuse et pourrait également réduire l’incidence des tumeurs malignes et des maladies auto-immunes associées à l’EBV”, a déclaré le directeur du NIAID, le Dr Anthony S. Fauci.
Dirigée par l’investigatrice principale Jessica Durkee-Shock, M.D., du Laboratoire des maladies infectieuses du NIAID, l’étude évaluera la sécurité et la réponse immunitaire d’un vaccin expérimental à base de nanoparticules de ferritine gp350 d’EBV avec un adjuvant Matrix-M à base de saponine. Le vaccin expérimental a été développé par le Laboratoire des maladies infectieuses en collaboration avec le Centre de recherche sur les vaccins du NIAID. L’adjuvant Matrix-M a été développé par la société de biotechnologie Novavax, basée à Gaithersburg, Maryland.
Le vaccin agit en ciblant la glycoprotéine gp350 de l’EBV, qui se trouve à la surface du virus et des cellules infectées par le virus. La gp350 de l’EBV est également la cible principale des anticorps neutralisants présents dans le sang des personnes naturellement infectées par l’EBV. La ferritine, une protéine naturelle de stockage du fer présente dans les cellules de toutes les espèces vivantes, est considérée comme une plateforme vaccinale prometteuse car elle peut afficher les protéines du virus ciblé en un réseau dense à sa surface. L’adjuvant est destiné à renforcer la réponse immunitaire induite par le vaccin expérimental.
L’étude portera sur 40 adultes volontaires en bonne santé âgés de 18 à 29 ans, dont la moitié présente des signes d’infection antérieure par le virus EBV et l’autre moitié n’a pas de signes d’infection antérieure par le virus EBV.. Les participants recevront une série de trois injections de 50 microgrammes du vaccin expérimental dans le muscle du bras, suivies de 30 à 60 minutes d’observation après chaque dose. Les deuxième et troisième doses seront administrées 30 jours et 180 jours après la dose initiale, avec des visites de suivi entre chaque vaccination et des appels téléphoniques entre les visites. La participation devrait être requise pendant 18 à 30 mois, et l’essai devrait durer quatre ans. De plus amples informations sur cette étude sont disponibles en utilisant l’identifiant NCT04645147 sur ClinicalTrials.gov.