Une équipe de chercheurs de l’Institut coréen des sciences et de la technologie a mis au point des “nanomachines”, qui utilisent des mouvements moléculaires mécaniques pour pénétrer dans les cellules et les détruire. La pénétration sélective des cellules cancéreuses est également possible en utilisant une molécule de verrouillage libérée à proximité des cellules cancéreuses.
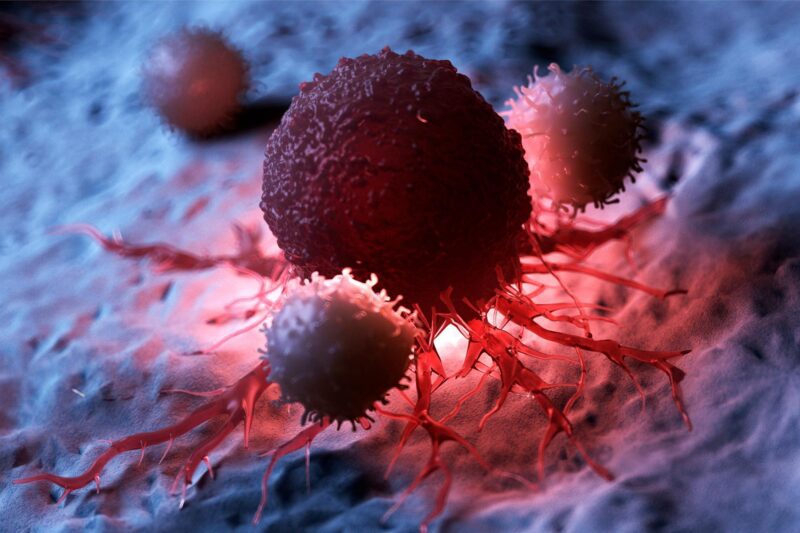
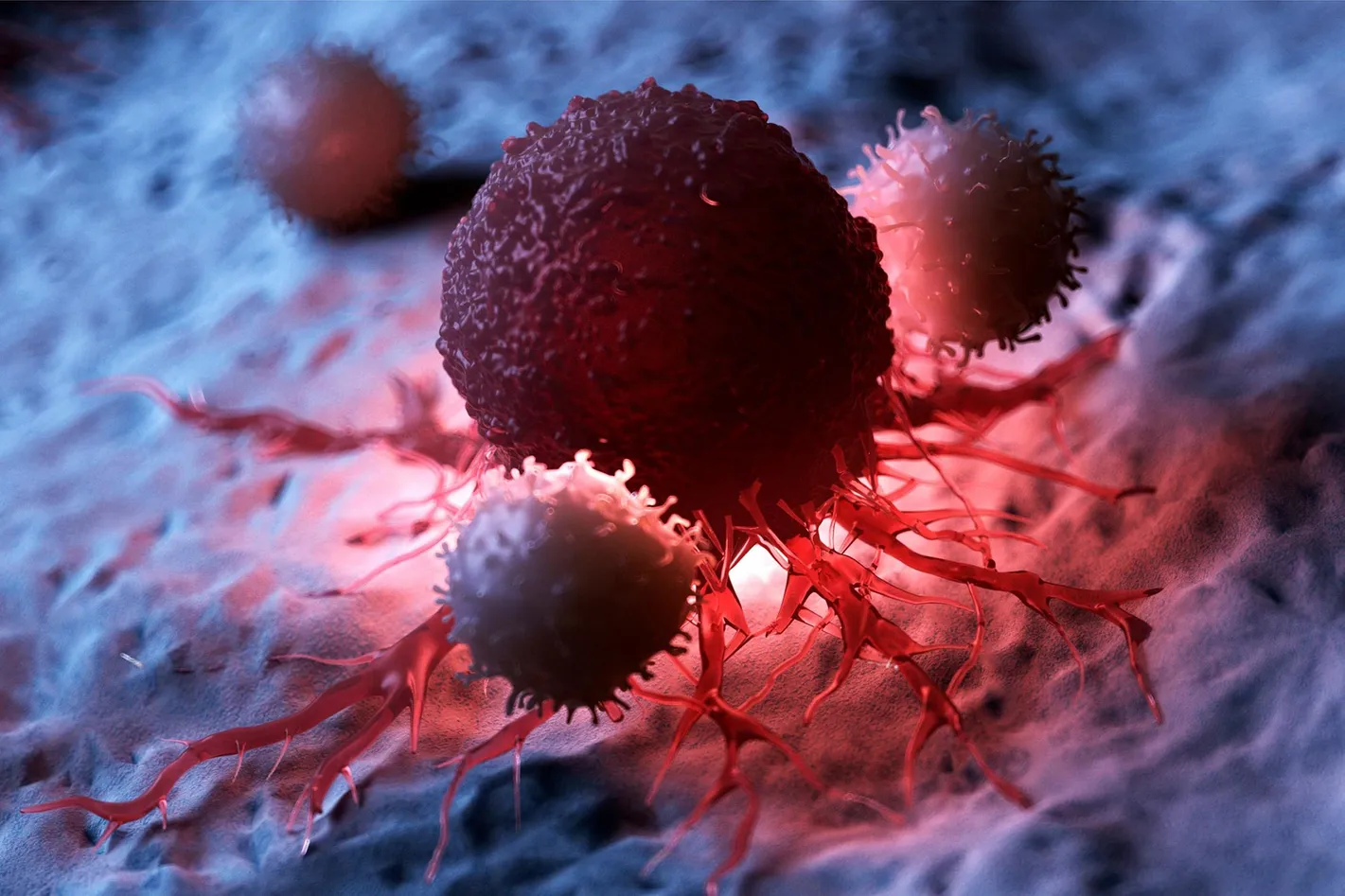
Des chercheurs ont créé des ‘nanomachines’ qui utilisent des mouvements moléculaires mécaniques pour pénétrer et détruire les cellules.
Le cancer est une maladie dans laquelle certaines cellules de l’organisme se développent de manière incontrôlée et se propagent à d’autres régions du corps. Les cellules cancéreuses se divisent continuellement, ce qui les amène à envahir les tissus environnants et à former des tumeurs solides. La majorité des traitements du cancer consistent à tuer les cellules cancéreuses.
Selon les estimations pour 2020, 1,8 million de nouveaux cas de cancer ont été diagnostiqués aux États-Unis, et 600 000 personnes sont décédées des suites de cette maladie. Le cancer du sein, le cancer du poumon, le cancer de la prostate et le cancer du côlon sont les cancers les plus courants. L’âge moyen d’un patient atteint de cancer au moment du diagnostic est de 66 ans, et les personnes âgées de 65 à 74 ans représentent 25 % de tous les nouveaux diagnostics de cancer.
Les protéines sont impliquées dans tous les processus biologiques et utilisent l’énergie du corps pour modifier leur structure par des mouvements mécaniques. On les qualifie de “nanomachines” biologiques, car même des modifications structurelles mineures des protéines ont un impact considérable sur les processus biologiques. Pour mettre en œuvre le mouvement dans l’environnement cellulaire, les chercheurs se sont concentrés sur le développement de nanomachines qui imitent les protéines. Cependant, les cellules utilisent une variété de mécanismes pour se défendre contre l’effet de ces nanomachines. Cela limite tout mouvement mécanique pertinent des nanomachines qui pourrait être utilisé à des fins médicales.
L’équipe de recherche dirigée par le Dr Youngdo Jeong du Centre de reconnaissance biomoléculaire avancée de l’Institut coréen des sciences et de la technologie (KIST) a rapporté le développement d’une nouvelle nanomachine biochimique qui pénètre la membrane cellulaire et tue la cellule via les mouvements moléculaires de pliage et de dépliage dans certains environnements cellulaires, comme les cellules cancéreuses. Ils ont collaboré avec les équipes du professeur Sang Kyu Kwak de l’école d’ingénierie énergétique et chimique et du professeur Ja-Hyoung Ryu du département de chimie de l’Institut national des sciences et technologies d’Ulsan (UNIST), ainsi qu’avec le Dr Chaekyu Kim de Fusion Biotechnology, Inc.

La nanomachine, développée par l’équipe de recherche conjointe KIST-UNIST, pénètre et tue sélectivement les cellules cancéreuses ainsi que son mécanisme d’action. Crédit : Institut coréen des sciences et de la technologie (KIST)
L’équipe de recherche conjointe s’est concentrée sur la structure hiérarchique des protéines, dans laquelle l’axe de la grande structure et les unités mobiles sont séparés hiérarchiquement. Par conséquent, seules des parties spécifiques peuvent se déplacer autour de l’axe. La plupart des nanomachines existantes ont été conçues de manière à ce que les composants mobiles et l’axe de la grande structure soient présents sur la même couche. Ainsi, ces composants subissent un mouvement simultané, ce qui complique le contrôle souhaité d’une partie spécifique.
Une nanomachine hiérarchique a été fabriquée en synthétisant et en combinant des nanoparticules d’or de 2 nm de diamètre avec des molécules qui peuvent être pliées et dépliées en fonction du milieu environnant. Cette nanomachine était composée de molécules organiques mobiles et de nanoparticules inorganiques fonctionnant comme des structures à grand axe et définissant le mouvement et la direction de telle sorte qu’en atteignant la membrane cellulaire, elle a entraîné un mouvement mécanique de pliage/dépliage qui a permis à la nanomachine de pénétrer directement dans la cellule, de détruire les organites et d’induire l’apoptose. Cette nouvelle méthode tue directement les cellules cancéreuses par des mouvements mécaniques sans médicament anticancéreux, contrairement aux nanocarriers de type capsule qui délivrent des médicaments thérapeutiques.
Par la suite, une molécule de verrouillage a été enfilée sur la nanomachine pour contrôler le mouvement mécanique et tuer sélectivement les cellules cancéreuses. La molécule de verrouillage enfilée a été conçue pour être libérée uniquement dans un environnement à faible pH. Par conséquent, dans les cellules normales dont le pH est relativement élevé (environ 7,4), les mouvements des nanomachines étaient limités et elles ne pouvaient pas pénétrer dans la cellule. Cependant, dans un environnement à faible pH autour des cellules cancéreuses (environ 6,8), les molécules de verrouillage ont été déliées, induisant un mouvement mécanique et la pénétration des cellules.
Le Dr Jeong a déclaré : “La nanomachine développée s’inspire des protéines qui remplissent des fonctions biologiques en modifiant leur forme en fonction de leur environnement. Nous proposons une nouvelle méthode de pénétration directe des cellules cancéreuses pour les tuer par le biais du mouvement mécanique.mouvements de molécules attachées à des nanomachines sans médicaments. Cela pourrait constituer une nouvelle alternative pour surmonter les effets secondaires des chimiothérapies existantes.”
Référence : “Stimuli-Responsive Adaptive Nanotoxin to Directly Penetrate the Cellular Membrane by Molecular Folding and Unfolding” par Youngdo Jeong, Soyeong Jin, L. Palanikumar, Huyeon Choi, Eunhye Shin, Eun Min Go, Changjoon Keum, Seunghwan Bang, Dongkap Kim, Seungho Lee, Minsoo Kim, Hojun Kim, Kwan Hyi Lee, Batakrishna Jana, Myoung-Hwan Park, Sang Kyu Kwak, Chaekyu Kim et Ja-Hyoung Ryu, 2 mars 2022, Journal of the American Chemical Society.
DOI : 10.1021/jacs.2c00084