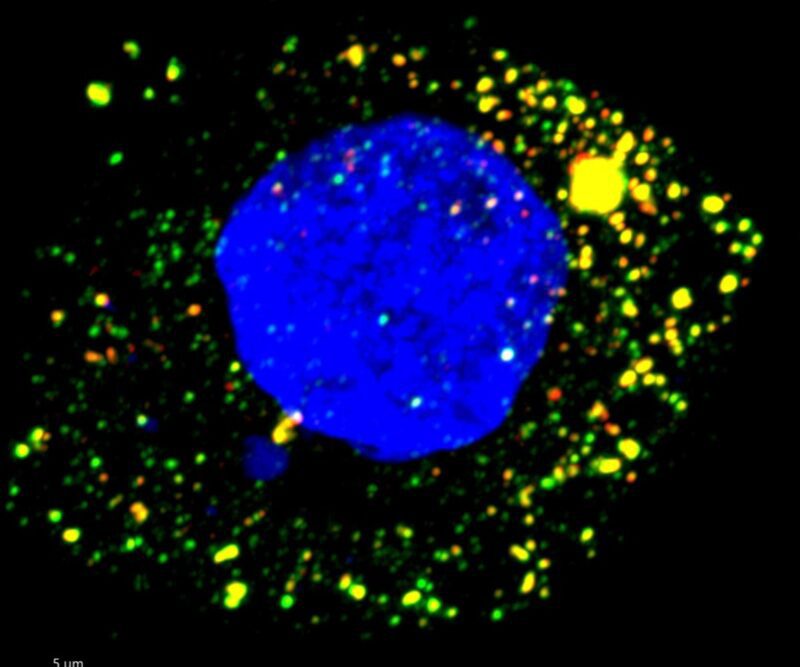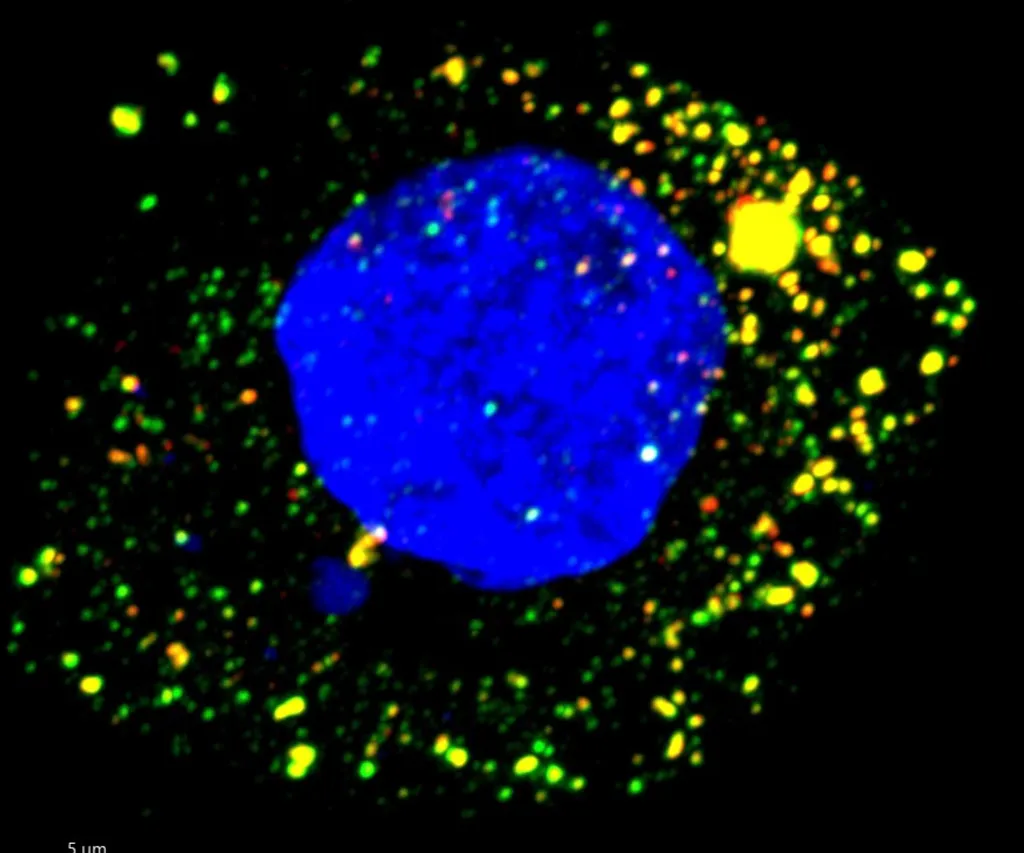
Image par microscopie à fluorescence d’une cellule hépatique humaine en culture infectée par le virus de l’hépatite A. L’ARN viral ciblé par ZCCHC14 apparaît en vert, et la protéine du virus en rouge. Crédit : Maryna Kapustina, École de médecine de l’UNC.
Des scientifiques découvrent la clé de la réplication du virus de l’hépatite A et démontrent l’efficacité du médicament.
En l’absence de traitement actuel de l’hépatite A, des scientifiques de l’école de médecine de l’Université de Caroline du Nord, sous la direction du docteur Stanley M. Lemon, ont découvert comment une protéine et des enzymes interagissent pour permettre au virus de l’hépatite A de proliférer.
Le cycle de réplication virale est essentiel pour qu’un virus se propage dans l’organisme et provoque une maladie. En se concentrant sur ce cycle dans le virus de l’hépatite A (VHA), les scientifiques de la faculté de médecine de l’Université de Caroline du Nord (UNC) ont découvert que la réplication nécessite des interactions particulières entre la protéine humaine ZCCHC14 et un groupe d’enzymes appelées polymérases poly(A) TENT4. Ils ont également découvert que le composé oral RG7834 arrêtait la réplication virale à une étape clé, empêchant ainsi l’infection des cellules du foie.
Ces résultats sont les premiers à démontrer un traitement médicamenteux efficace contre le VHA dans un modèle animal de la maladie. L’étude a été publiée aujourd’hui (4 juillet 2022) dans la revue . Proceedings of the National Academy of Sciences.
“Notre recherche démontre que le ciblage de ce complexe protéique avec une petite molécule thérapeutique administrée par voie orale arrête la réplication virale et inverse l’inflammation du foie dans un modèle de souris de l’hépatite A, fournissant une preuve de principe pour la thérapie antivirale et les moyens d’arrêter la propagation de l’hépatite A dans les situations d’épidémie “, a déclaré l’auteur principal Stanley M. Lemon, MD, professeur au Département de médecine et au Département de microbiologie et d’immunologie de l’UNC, et membre de l’Institut de l’UNC pour la santé mondiale et les maladies infectieuses.
Lemon, qui, dans les années 1970 et 1980, faisait partie d’une équipe de recherche du Walter Reed Army Medical Center qui a mis au point le premier vaccin inactivé contre le VHA administré à l’homme, a déclaré que la recherche sur le VHA a diminué après que le vaccin soit devenu largement disponible au milieu des années 1990. Les cas ont chuté dans les années 2000, alors que les taux de vaccination montaient en flèche. Les chercheurs se sont alors tournés vers les virus de l’hépatite B et C, qui sont tous deux très différents du VHA et provoquent des maladies chroniques. “C’est comme comparer des pommes à des navets”, a déclaré Mme Lemon. “La seule similitude est qu’ils provoquent tous une inflammation du foie”. Le VHA ne fait même pas partie de la même famille de virus que les virus de l’hépatite B et C.
Les épidémies d’hépatite A sont en hausse depuis 2016, même si le vaccin contre le VHA est très efficace. Tout le monde ne se fait pas vacciner, a souligné Mme Lemon, et le VHA peut exister pendant de longues périodes dans l’environnement – comme sur nos mains et dans la nourriture et l’eau – ce qui a entraîné plus de 44 000 cas, 27 000 hospitalisations et 400 décès aux États-Unis depuis 2016, selon l’… CDC.
Plusieurs épidémies ont eu lieu au cours des dernières années, notamment à San Diego en 2017 motivée en grande partie par l’itinérance et la consommation de drogues illicites, provoquant une maladie grave chez environ 600 personnes et en tuant 20. En 2022, une petite épidémie a eu lieu. liée à des fraises biologiques dans plusieurs États, entraînant une douzaine d’hospitalisations. Une autre épidémie en 2019 a été liée à des mûres fraîches. Dans le monde, des dizaines de millions d’infections par le VHA se produisent chaque année. Les symptômes sont la fièvre, les douleurs abdominales, la jaunisse, les nausées et la perte d’appétit et du sens du goût. Une fois malade, il n’y a pas de traitement.
En 2013, Lemon et ses collègues ont découvert que le virus de l’hépatite A change radicalement à l’intérieur du foie humain. Le virus détourne des morceaux de membrane cellulaire lorsqu’il quitte les cellules du foie, se dissimulant ainsi des anticorps qui auraient autrement mis le virus en quarantaine avant qu’il ne se propage largement dans le sang. Ce travail a été publié dansNature et ont permis de comprendre tout ce que les chercheurs avaient encore à apprendre sur ce virus découvert il y a 50 ans et qui est probablement à l’origine de maladies remontant aux temps anciens.
Il y a quelques années, les chercheurs ont découvert que le virus de l’hépatite B avait besoin de TENT4A/B pour sa réplication. Pendant ce temps, le laboratoire de Lemon a mené des expériences pour rechercher les protéines humaines dont le VHA a besoin pour se répliquer, et ils ont trouvé ZCCHC14 – une protéine particulière qui interagit avec le zinc et se lie à RNA.
“This was the tipping point for this current study,” Lemon said. “We found ZCCHC14 binds very specifically to a certain part of HAV’s RNA, the molecule that contains the virus’s genetic information. And as a result of that binding, the virus is able to recruit TENT4 from the human cell.”
In normal human biology, TENT4 is part of an RNA-modification process during cell growth. Essentially, HAV hijacks TENT4 and uses it to replicate its own genome.
This work suggested that stopping TENT4 recruitment could stop viral replication and limit disease. Lemon’s lab then tested the compound RG7834, which had previously been shown to actively block Hepatitis B virus by targeting TENT4. In the PNAS paper, the researchers detailed the precise effects of oral RG7834 on HAV in liver and feces and how the virus’s ability to cause liver injury is dramatically diminished in mice that had been genetically modified to develop HAV infection and disease. The research suggests the compound was safe at the dose used in this research and the acute timeframe of the study.
“This compound is a long way from human use,” Lemon said, “But it points the path to an effective way to treat a disease for which we have no treatment at all.”
The pharmaceutical company Hoffmann-La Roche developed RG7834 for use against chronic hepatitis B infections and tested it in humans in a phase 1 trial, but animal studies suggested it may be too toxic for use over long periods of time.
“The treatment for Hepatitis A would be short term,” Lemon said, “and, more importantly, our group and others are working on compounds that would hit the same target without toxic effects.”
Reference: “The ZCCHC14/TENT4 complex is required for hepatitis A virus RNA synthesis” 4 July 2022, Proceedings of the National Academy of Sciences.
DOI: 10.1073/pnas.2204511119
This research was a collaboration between the Lemon lab and the lab of Jason Whitmire, professor of genetics at the UNC School of Medicine. Lemon and Whitmire are members of the UNC Lineberger Comprehensive Cancer Center.
First authors of the PNAS paper are You Li and Ichiro Misumi. Other authors, all at UNC, are Tomoyuki Shiota, Lu Sun, Erik Lenarcic, Hyejeong Kim, Takayoshi Shirasaki, Adriana Hertel-Wulff, Taylor Tibbs, Joseph Mitchell, Kevin McKnight, Craig Cameron, Nathaniel Moorman, David McGivern, John Cullen, Jason K. Whitmire, and Stanley M. Lemon.
This work was supported by grants from the National Institute of Allergy and Infectious Diseases (R01-AI131685), (R01-AI103083), (R01-AI150095), (R21-AI163606), (R01-AI143894), (R01-AI138337). The UNC Pathology Services Core and UNC High-Throughput Sequencing Facility were supported in part by a National Cancer Institute Center Core Support Grant (P30CA016086) to the UNC Lineberger Comprehensive Cancer Center.