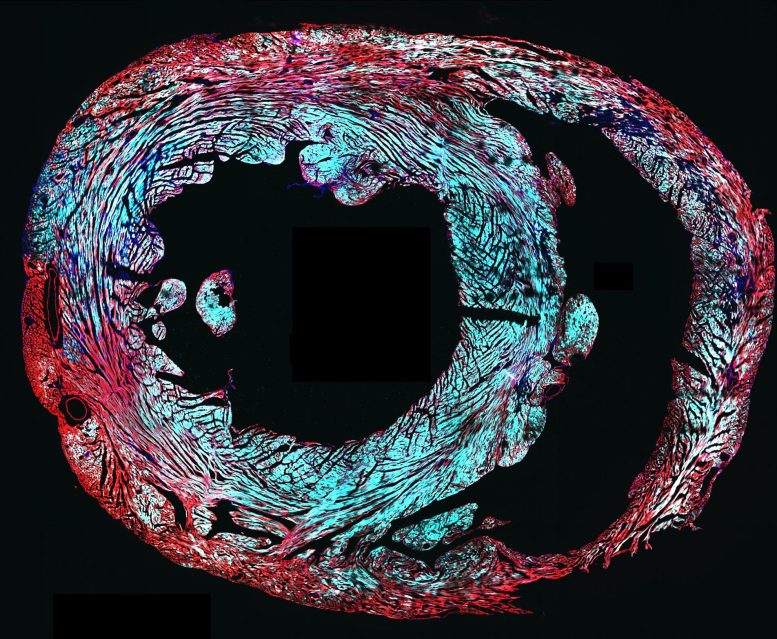
Cette coupe transversale d’un cœur de souris (rouge) montre à quel point la thérapie génique a permis de délivrer les gènes du canal ionique du sodium (cyan) aux cellules cardiaques cibles après que les chercheurs ont injecté un virus contenant les gènes dans les veines de la souris. Crédit : Tianyu Wu, Université de Duke
La première approche visant à promouvoir l’excitation électrique des cellules cardiaques chez les mammifères vivants pourrait conduire à de nouveaux traitements de thérapie génique pour un large éventail de maladies cardiaques.
Les ingénieurs biomédicaux de l’Université Duke ont démontré une thérapie génique qui aide les cellules du muscle cardiaque à s’activer électriquement chez des souris vivantes. Première démonstration de ce type, cette approche fait appel à des gènes bactériens modifiés qui codent pour les canaux ioniques du sodium et pourrait conduire à des thérapies pour traiter une grande variété de maladies et de troubles cardiaques électriques.
Les résultats sont apparus en ligne le 2 février 2022 dans la revue Nature Communications.
“Nous avons pu améliorer la capacité des cellules du muscle cardiaque à initier et à propager l’activité électrique, ce qui est difficile à réaliser avec des médicaments ou d’autres outils”, a déclaré Nenad Bursac, professeur d’ingénierie biomédicale à Duke. “La méthode que nous avons utilisée pour délivrer des gènes dans les cellules du muscle cardiaque des souris a déjà montré qu’elle persistait pendant une longue période, ce qui signifie qu’elle pourrait aider efficacement les cœurs qui luttent pour battre aussi régulièrement qu’ils le devraient.”
Les canaux sodium-ion sont des protéines situées dans les membranes externes des cellules électriquement excitables, comme les cellules cardiaques ou cérébrales, qui transmettent les charges électriques dans la cellule. Dans le cœur, ces canaux indiquent aux cellules musculaires quand se contracter et transmettent l’instruction de sorte que l’organe pompe le sang comme une unité cohérente. Cependant, les cellules cardiaques endommagées, que ce soit par une maladie ou un traumatisme, perdent souvent tout ou partie de leur capacité à transmettre ces signaux et à se joindre à l’effort.
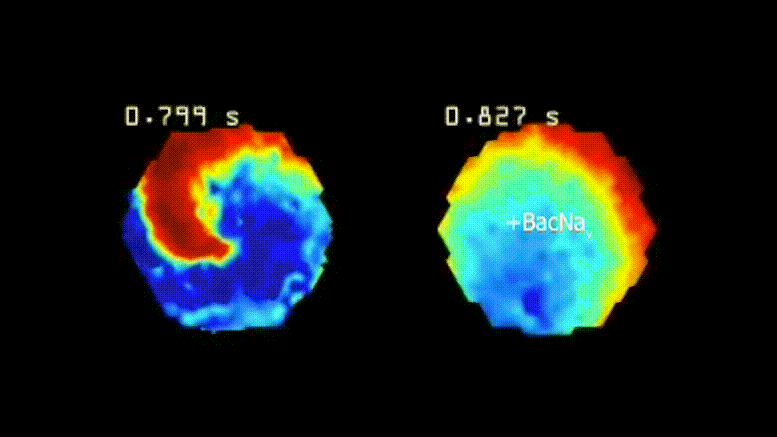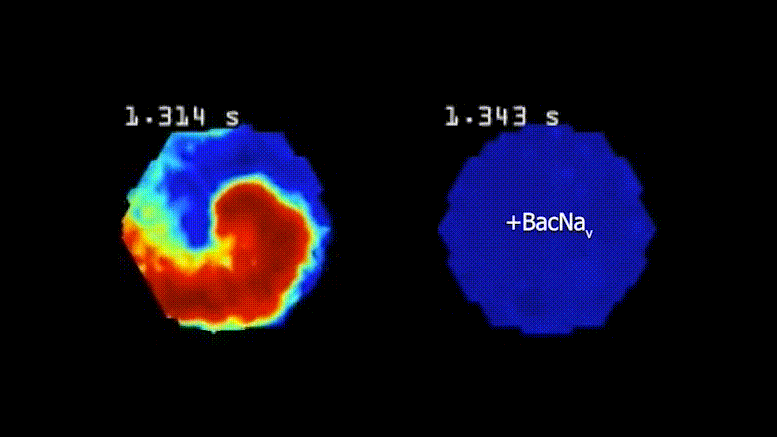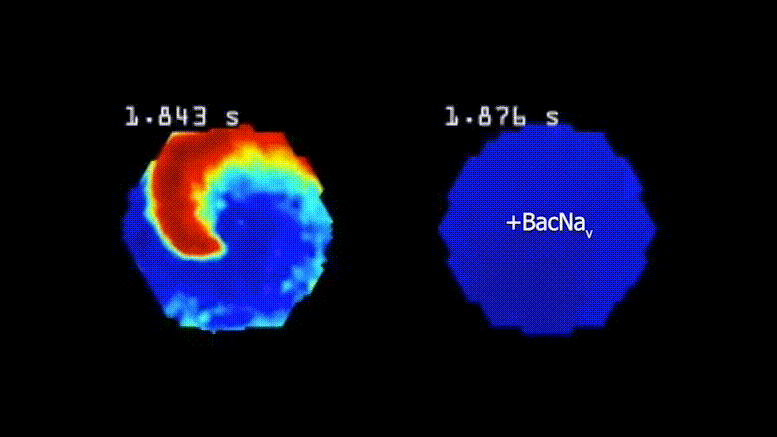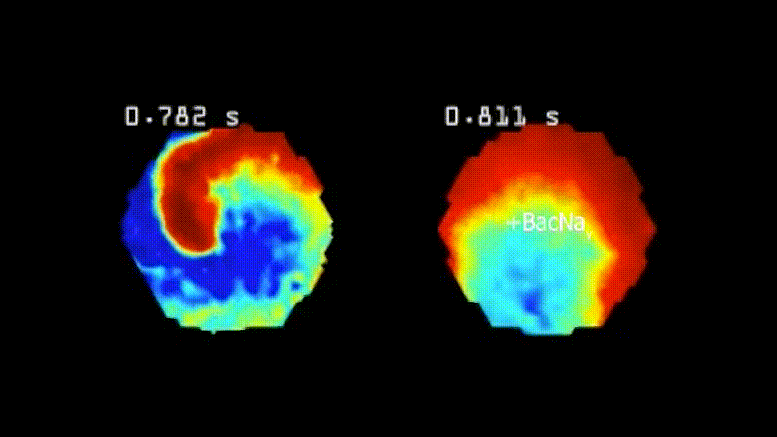
Les arythmies cardiaques se produisent lorsque les cellules du muscle cardiaque ne transmettent pas uniformément les signaux électriques pour pomper le sang de manière cohérente et ordonnée. La vidéo de gauche montre des cellules arythmiques dans un chaos de tachycardie, tandis que la vidéo de droite montre des cellules traitées par la nouvelle thérapie génique se comportant normalement, car il est beaucoup plus difficile de les pousser hors de leur activité régulière de battement cardiaque. Crédit : Tianyu Wu, Université Duke
La thérapie génique est l’une des approches que les chercheurs peuvent adopter pour rétablir cette fonctionnalité. En délivrant les gènes responsables de la création des protéines des canaux sodiques, la technique permet de produire davantage de canaux ioniques dans les cellules malades afin de stimuler leur activité.
Chez les mammifères, les gènes des canaux sodiques sont malheureusement trop gros pour tenir dans les virus actuellement utilisés dans les thérapies géniques modernes chez l’homme. Pour contourner ce problème, Bursac et son laboratoire se sont tournés vers des gènes plus petits qui codent pour des canaux ioniques sodiques similaires chez les bactéries. Bien que ces gènes bactériens soient différents de leurs homologues humains, l’évolution a conservé de nombreuses similitudes dans la conception du canal depuis que les organismes pluricellulaires ont divergé des bactéries il y a des centaines de millions d’années.
Il y a plusieurs années, Hung Nguyen, un ancien doctorant du laboratoire de Bursac qui travaille maintenant pour Fujifilm Diosynth Biotechnologies, a muté ces gènes bactériens afin que les canaux qu’ils codent puissent devenir actifs dans les cellules humaines. Dans le cadre de ces nouveaux travaux, l’actuel doctorant Tianyu Wu a encore optimisé le contenu des gènes et les a associés à un “promoteur” qui limite exclusivement la production des canaux aux cellules du muscle cardiaque. Les chercheurs ont ensuite testé leur approche en administrant un virus chargé du gène bactérien dans les veines d’une souris pour qu’il se propage dans tout le corps.
“Nous avons cherché à savoir où les canaux ioniques sodiques étaient effectivement formés et, comme nous l’espérions, nous avons constaté qu’ils n’étaient présents que dans les cellules musculaires actives du cœur, dans les oreillettes et les ventricules”, a déclaré Wu. “Nous avons également constaté qu’ils ne se retrouvaient pas dans les cellules cardiaques à l’origine des battements du cœur, ce que nous voulions également éviter.”
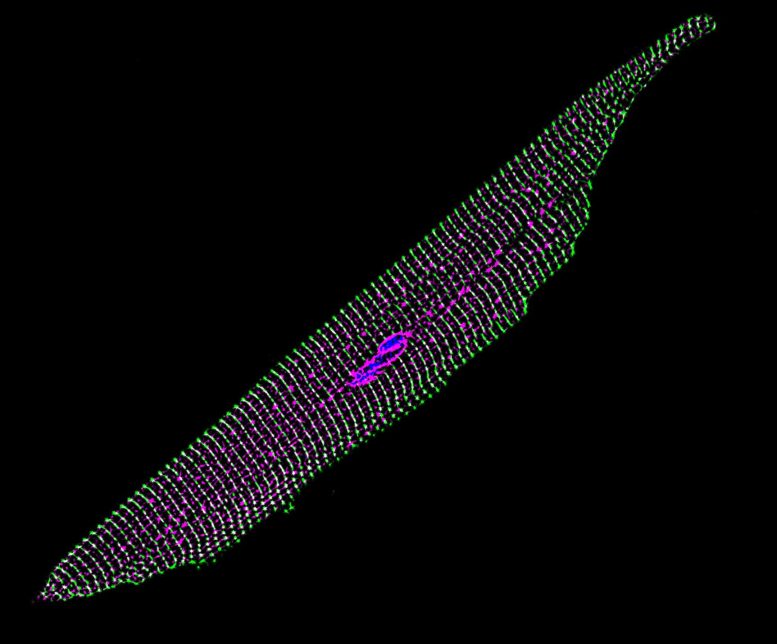
Cette image détaillée d’une seule cellule du muscle cardiaque d’une souris montre sa membrane cellulaire exprimant les nouveaux gènes de canal ionique sodique (magenta) après que les chercheurs ont administré la thérapie par une injection dans les veines de la souris. Crédit : Tianyu Wu, Université Duke
Cette approche de la thérapie génique ne fait qu’apporter des gènes supplémentaires dans une cellule ; elle ne tente pas de couper, de remplacer ou de réécrire les DNA in any way. Scientists believe these types of delivered genes make proteins while floating freely within the cell, making use of the existing biochemical machinery. Previous research with this viral gene delivery approach suggests the transplanted genes should remain active for many years.
As a proof of concept, tests on cells in a laboratory setting suggest that the treatment improves electrical excitability enough to prevent human abnormalities like arrhythmias. Within live mice, the results demonstrate that the sodium ion channels are active in the hearts, showing trends toward improved excitability. However, further tests are needed to measure how much of an improvement is made on the whole-heart level, and whether it is enough to rescue electrical function in damaged or diseased heart tissue to be used as a viable treatment.
Moving forward, the researchers have already identified different bacterial sodium channel genes that work better in preliminary benchtop studies. The team is also working with the laboratories of Craig Henriquez, professor of biomedical engineering at Duke, and Andrew Landstrom, director of the Duke Pediatric Research Scholars Program, to test the ability of these genes to restore heart functionality in mouse models that mimic human heart diseases.
“I think this work is really exciting,” Bursac said. “We have been harnessing what nature made billions of years ago to help humans with modern-day disease.”
Reference: “Engineered Bacterial Voltage-Gated Sodium Channel Platform for Cardiac Gene Therapy” by Hung X. Nguyen, Tianyu Wu, Daniel Needs, Hengtao Zhang, Robin M. Perelli, Sophia DeLuca, Rachel Yang, Michael Tian, Andrew P. Landstrom, Craig Henriquez and Nenad Bursac, 2 February 2022. Nature Communications.
DOI: 10.1038/s41467-022-28251-6
This work was supported by the National Institutes of Health (HL134764, HL132389, HL126524, 1U01HL143336-01), the Duke Translating Duke Health Initiative, and the American Heart Association Predoctoral Fellowship (829638).


