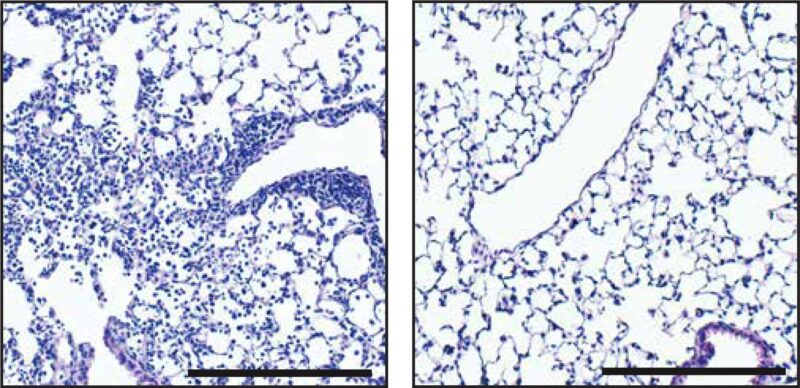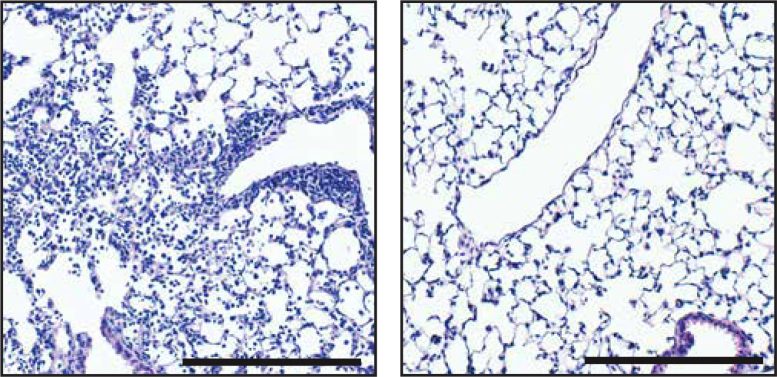
Comparé à un contrôle (à gauche), le traitement avec le SLR14 (à droite) réduit les signes d’inflammation et de pneumonie dans les poumons des souris infectées par le SRAS-CoV-2. Crédit : ©2021 Mao et al. Publié à l’origine dans Journal de médecine expérimentale. https://doi.org/10.1084/jem.20211818
Des chercheurs de la Yale School of Medicine ont découvert qu’un ARN molécule qui stimule le système de défense antivirale précoce du corps peut protéger les souris contre une gamme de SRAS-CoV-2 variantes. L’étude, publiée récemment dans le Journal de médecine expérimentale (JEM), pourrait conduire à de nouveaux traitements pour COVID-19[feminine chez les patients immunodéprimés, tout en offrant une option thérapeutique peu coûteuse pour les pays en développement qui n’ont actuellement pas accès aux vaccins.
Bien que les vaccins approuvés contre le SRAS-CoV-2 soient très efficaces pour prévenir les maladies graves et les décès pendant la pandémie de COVID-19 en cours, la disponibilité des vaccins est extrêmement limitée dans de nombreux pays à faible revenu, et de nouvelles souches du virus résistantes aux vaccins pourraient émerger à l’avenir. De plus, l’efficacité des vaccins est déjà réduite chez les individus immunodéprimés incapables de former un nombre suffisant d’anticorps ou de cellules T qui ciblent spécifiquement la protéine de pointe virale. Ces personnes sont sensibles aux infections chroniques à long terme par le SRAS-CoV-2.
« C’est pourquoi, en plus de l’utilisation de vaccins pour prévenir le COVID-19, des efforts sont nécessaires pour développer des thérapies efficaces contre le SRAS-CoV-2 », explique Akiko Iwasaki, professeur à la Yale School of Medicine.
On pense que la première ligne de défense du corps contre le SRAS-CoV-2 – avant l’implication des anticorps et des cellules T – dépend de molécules réceptrices telles que RIG-I qui reconnaissent le matériel génétique du virus et induisent la production de protéines de signalisation connues sous le nom de type J’interférons. Ces interférons, à leur tour, favorisent la production de protéines qui peuvent inhiber la réplication virale et stimuler le recrutement de cellules immunitaires pour combattre l’infection.
De nombreuses études ont suggéré qu’une production précoce et robuste d’interférons protège contre le COVID-19, tandis qu’une production retardée est associée à une maladie grave. Un essai clinique a montré que le traitement des patients COVID-19 avec une protéine d’interféron purifiée au début de la maladie peut réduire la mortalité, mais la fabrication d’interférons est extrêmement coûteuse.
Dans le nouveau JEM étude, Iwasaki et ses collègues suggèrent une alternative moins chère : traiter les patients avec de courtes molécules d’ARN qui imitent le matériel génétique du SRAS-CoV-2 et activent le récepteur RIG-I pour stimuler la production d’interférons de type I par les propres cellules du corps.
Les chercheurs ont testé leur approche sur des souris sensibles à l’infection par le SRAS-CoV-2. Une seule dose d’une molécule d’ARN nommée SLR14 était suffisante pour protéger les souris d’une maladie grave et de la mort, en particulier si le traitement était administré peu de temps avant ou peu après l’exposition au virus. Lorsqu’il est administré peu de temps après l’infection virale, le SLR14 s’est avéré plus efficace que le traitement de souris avec une protéine d’interféron purifiée, ont déterminé les chercheurs.
Surtout, le SLR14 a protégé les souris de toutes les variantes émergentes du SRAS-CoV-2, y compris la variante delta responsable de la récente augmentation des cas de COVID-19 aux États-Unis.
Enfin, Iwasaki et ses collègues ont testé le SLR14 chez des sujets immunodéprimés Chiffon–/– souris infectées de façon chronique par le SRAS-CoV-2. La molécule d’ARN a pu éliminer complètement le virus de ces animaux, même s’ils manquent à la fois de cellules T et de cellules B productrices d’anticorps.
Iwasaki et ses collègues soulignent que les molécules d’ARN comme SLR14 sont relativement bon marché et faciles à fabriquer. « Le SLR14 est donc très prometteur en tant que nouvelle classe de thérapies à ARN pouvant être appliquées comme antiviraux contre le SRAS-CoV-2 », a déclaré Iwasaki. “De plus, parce que cette approche thérapeutique basée sur l’ARN est simple et polyvalente, notre étude facilitera la préparation et la réponse à une pandémie contre les futurs agents pathogènes respiratoires sensibles aux interférons de type I.”
Référence : « A stem-loop RNA RIG-I agoniste protège contre l’infection aiguë et chronique du SRAS-CoV-2 chez la souris » par Tianyang Mao, Benjamin Israelow, Carolina Lucas, Chantal BF Vogels, Maria Luisa Gomez-Calvo, Olga Fedorova, Mallery I. Breban, Bridget L. Menasche, Huiping Dong, Melissa Linehan, Yale SARS-CoV-2 Genome Surveillance Initiative, Craig B. Wilen, Marie L. Landry, Nathan D. Grubaugh, Anna M. Pyle et Akiko Iwasaki, 10 novembre 2021, Journal de médecine expérimentale (JEM).
DOI : 10.1084 / jem.20211818